在恒温、恒压下,a mol A和b molB在一个容积可变的容器中发生反应:A(g) +2B(g) 2C(g),一段时间后达到平衡,生成n mol C。下列说法正确的
2C(g),一段时间后达到平衡,生成n mol C。下列说法正确的
A.物质A、B的转化率之比为l:2
B.起始时刻和达到平衡后容器中的压强之比为(a+b):(a+b-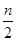 )
)
C.当v正(A)=v逆(B)时,反应一定达到平衡状态
D.充入惰性气体,平衡向逆反应方向移动
一定温度下在容积恒定的密闭容器中,进行如下可逆反应:A(s)+2B(g) C(g)+D(g),下列叙述能表明该反应已达到平衡状态的是()
C(g)+D(g),下列叙述能表明该反应已达到平衡状态的是()
①混合气体的密度不再变化时②容器内气体的压强不再变化时
③混合气体的总物质的量不再变化时④ B物质的量浓度不再变化时
⑤当V正(C) = V逆(D) 时⑥当V正(B) = 2V逆(C)
A.①④⑤⑥ B.②③⑥ C.②④⑤⑥ D.只有④
一个原电池的总反应离子方程式是Zn + Cu2+ = Zn2+ + Cu,该反应的原电池组成正确()
| A |
B |
C |
D |
|
| 正极 |
Zn |
Ag |
Cu |
Cu |
| 负极 |
Cu |
Cu |
Zn |
Zn |
| 电解质溶液 |
CuCl2 |
H2S04 |
CuSO4 |
FeCl2 |
关于氢键的下列说法中正确的是()
| A.每个水分子内含有两个氢键 |
| B.在水蒸气、水和冰中都含有氢键 |
| C.分子间能形成氢键使物质的熔点和沸点升高 |
| D.HF的稳定性很强,是因为其分子间能形成氢键 |
甲、乙两种非金属:
①甲比乙容易与H2化合;
②甲单质能与乙阴离子发生置换反应
③甲的最高价氧化物对应的水化物酸性比乙的最高价氧化物对应的水化物酸性强;
④ 与某金属反应时,甲原子得电子数目比乙的多;
⑤甲的单质熔、沸点比乙的低。能说明甲比乙的非金属性强的是()
| A.只有④ | B.只有⑤ | C.①②③ | D.①②③④⑤ |
直接提供电能的反应一般是放热反应,下列反应中能提供电能的是()
| A.Ba(OH)2·8H2O与NH4Cl反应 | B.氢氧化钠与稀盐酸反应 |
| C.灼热的炭与CO2反应 | D.H2与Cl2燃烧反应 |