纯碱和小苏打都是白色晶体,在日常生活中都可以找到。若要在家中将它们区分开来,下面的方法中可行的是
| A.在水杯中各盛相同质量的样品,分别加入等体积的白醋,观察反应的剧烈程度 |
| B.分别用干净铁丝蘸取样品在煤气炉的火焰上灼烧,观察火焰颜色 |
| C.将样品溶解,分别加入澄清石灰水,观察是否有白色沉淀 |
| D.分别放在炒锅中加热,观察是否有残留物 |
我国科学家在世界上第一次为一种名为“钴酞箐”的分子(直径为1.3×10-9m)恢复了磁性。“钴酞箐”分子的结构和性质与人体内的血红素和植物的叶绿素非常相似。下列关于“钴酞箐”分子的说法中正确的是()
A.它的分子直径比Na+小 |
B.它的分子既能透过滤纸,也能透过半透膜 |
C.在水中形成的分散系能产生丁达尔效应 |
| D.在水中所形成的分散系属悬浊液 |
下列有关苯酚的叙述中不正确的是()
| A.苯酚是酸,它能与NaOH溶液反应 | B.苯酚钠溶液中通入CO2气体可得苯酚 |
| C.苯中混有的少量苯酚可用乙醇除去 | D.苯酚有毒,但药皂中常掺有少量苯酚 |
下列反应能说明苯酚分子中由于羟基影响苯环使苯酚分子中苯环比苯活泼的是()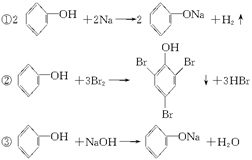
| A.①和③ | B.只有② | C.②和③ | D.全部 |
仅用一种试剂即可将酒精、苯酚溶液、乙烯、甲苯4种无色液体区分开来,这种试剂是()
| A.FeCl3溶液 | B.溴水 | C.KMnO4溶液 | D.金属钠 |
已知①通常Br2与“ ”双键起加成反应,但高温下Br2易取代与“
”双键起加成反应,但高温下Br2易取代与“ ”双键直接相连的α-碳原子上的氢原子:
”双键直接相连的α-碳原子上的氢原子: +HBr
+HBr
②与苯环直接相连的支链碳原子上的氢原子也易被溴取代: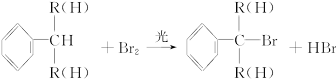
根据以上信息写出从正丙苯
( )制取1苯基丙三醇(C6H5—CHOH—CHOH—CH2OH)的各步反应的化学方程式(注明条件)。
)制取1苯基丙三醇(C6H5—CHOH—CHOH—CH2OH)的各步反应的化学方程式(注明条件)。