以下是一些原子的2p能级和3d能级中电子排布的情况。其中违反了洪特规则的是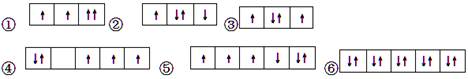
| A.① | B.①③ | C.②④⑤ | D.③④⑤ |
对于达到平衡的反应:2A(g)+B(g)⇌nC(g),符合如图所示的结论是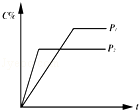
| A.P1>P2,n>3 | B.P1>P2,n<3 | C.P1<P2,n>3 | D.P1<P2,n<3 |
利用反应:2NO(g)+2CO(g)⇌2C02(g)+N2(g)△H=﹣746.8kJ•mol﹣1,可净化汽车尾气,如果要同时提高反应的速率和N0的转化率,采取的措施是
| A.降低温度 |
| B.增大压强 |
| C.升高温度同时充入N2 |
| D.及时将C02和N2从反应体系中移走 |
在一密闭烧瓶中,在25℃时存在着平衡:2NO2⇌N2O4(正反应放热).把烧瓶置于100℃的水中,则下列几项性质中不会改变的是
①颜色;②平均分子量;③质量;④压强;⑤密度
| A.①和③ | B.②和④ | C.④和⑤ | D.③和⑤ |
下列说法正确的是
| A.甲烷的燃烧热为﹣890.3kJ•mol﹣1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=﹣890.3kJ•mol﹣1 |
| B.NaOH(aq)+CH3COOH (aq)=CH3COONa(aq)+H2O(l)△H=﹣57.3kJ/mol (中和热) |
| C.测定HCl和NaOH反应的中和热时,每次实验均应测量3个温度,即盐酸起始温度、NaOH起始温度和反应后终止温度 |
| D.2H2 (g)+O2(g)=2H2O(l) △H=﹣571.6kJ/mol (燃烧热) |
下列反应属于吸热反应的是
A.C6H12O6(葡萄糖)+6O2 6CO2+6H2O 6CO2+6H2O |
| B.HCl+KOH═KCl+H2O |
| C.反应物的总能量大于生成物的总能量 |
| D.破坏反应物全部化学键所需能量大于破坏生成物全部化学键所需能量 |