三种金属单质A、B、C与气体甲、乙、丙及物质D、E、F、G、H之间发生如下转化关系(图中有些反应的产物和反应的条件没有标出)。请根据以上信息回答下列问题:
(1)写出下列物质的化学式:
A_____、乙____ ,C的一种氧化物是具有磁性的黑色晶体,该氧化物的化学式是__________。
(2)写出反应②的化学方程式: ____________________。
短周期元素A、B、C、D ,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构;两元素的单质反应,生成一种淡黄色的固体E;D的L层电子数等于K、M两电子层上电子数之和。
(1)元素:A为:B为:C为:
(2)D的质子数和中子数相等。D 的原子组成符号为:它的最高价氧化物对应的水化物的化学式为:。
(3)用电子式表示A、B两元素形成AB2的过程:,用电子式表示C、D两元素形成化学键的过程:
下列变化中①NaCl 溶于水②HCl 溶于水③O2 溶于水④Na2O2溶于水⑤I2升华⑥固体NaOH熔化。未发生化学键破坏的是仅发生离子键破坏的是,仅发生共价键破坏的是既发生离子键破坏,又发生共价键破坏的是(填序号)。
现有下列基本粒子:1H、2H、3H、1H+、40K、40Ca、Cl2、14N、14C,请回答问题:
(1)它们分属种元素,互为同位素的原子为。
(2)质量数相等的粒子为、、(可不填满,也可补充)。
(3)氢的同位素1H、2H、3H与氧的同位素16O、17O、18O相互结合为水,可得水分子的种数为;可得相对分子质量不同的水分子种数为。
第一电离能I1是指气态原子X(g)失去一个电子成为气态阳离子X+(g)所需的能量。下图是部分元素原子的第一电离能I1随原子序数变化的曲线图。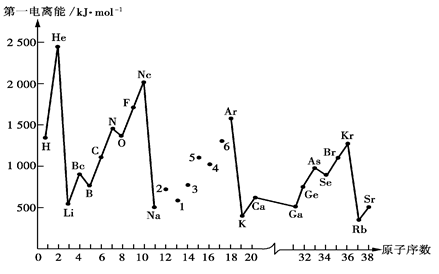
请回答以下问题:
(1)认真分析上图中同周期元素第一电离能的变化规律,将Na——Ar之间六种元素用短线连接起来,构成完整的图像。
(2)从上图分析可知,同一主族元素原子的第一电离能I1变化规律是__________________________;
(3)上图中5号元素在周期表中的位置是___________________________;
(4)上图中4、5、6三种元素的气态氢化物的沸点与同主族上一周期的元素的氢化物比(对应NH3 H2O HF)的沸点低的原因:__________________________________
本题包括两道题
(1)下面是s能级p能级的原子轨道图,试回答问题:
s电子的原子轨道呈形,每个s能级有个原子轨道;
p电子的原子轨道呈形,每个p能级有个原子轨道。
(2)A、B、C、D、E都是元素周期表中前20号的元素,原子序数依次增大,B、C、D同周期,A、D同主族,E和其它元素既不在同周期也不在同主族,B、C、D的最高价氧化物的水化物两两混合均能发生反应生成盐和水。A和E可组成离子化合物,其晶胞(晶胞是在晶体中具有代表性的最小重复单元)结构如下图所示,阳离子(用“●”表示)位于该正方体的顶点或面心;阴离子(用“○”表示)位于小正方体的中心。
根据以上信息,回答下列问题:A至E的元素名称:
A;B;C;D;E