有机物A可以通过不同的反应得到B和C: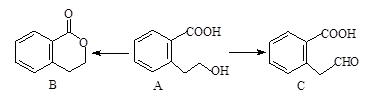
(1)A的分子式为 ,C的含氧官能团名称为 。
(2)A制取B的有机反应类型为 ;A制取C的化学方程式为: 。
(3)A发生消去反应后产物的结构简式为 ,A分子中一定共面的碳原子有 个。
(4)芳香族化合物D是A的同分异构体,1molD可以和3mol NaOH发生中和反应;D苯环
上的一氯代物只有一种且分子中没有甲基。请写出D的结构简式 (任写一种)。
已知:还原性HSO3->I-,氧化性IO3-> I2 。
(1)在NaIO3溶液中滴加少量NaHSO3溶液,发生下列反应。配平反应方程式并标出电子转移的方向和数目。
囗NaIO3+囗NaHSO3 → 囗I2+囗Na2SO4+囗H2SO4+囗H2O
(2)在NaIO3溶液中滴加过量NaHSO3溶液,反应完全后,推测反应后 溶液中的还原产物为_________(填化学式);
溶液中的还原产物为_________(填化学式);
(3)在含5molNaHSO3的溶液中逐滴加入NaIO3溶液。加入NaIO3的物质的量和析出I2单质的物质的 量的关系曲线如图所示。写出反应过程中与AB段曲线对应的离子方程式__________________________;当溶液中I-与I2的物质的量之比为5:3时,加入的NaIO3为mol。
量的关系曲线如图所示。写出反应过程中与AB段曲线对应的离子方程式__________________________;当溶液中I-与I2的物质的量之比为5:3时,加入的NaIO3为mol。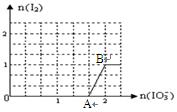
根据元素周期表及周期律的知识回答下列问题:
(1)与钠同周期且离子半径最小的元素位于周期表的第________________族。其氧化物属于________晶体。
(2)金属钠在一定条件下与氢气反应生成氢化钠(2Na+H2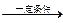 2NaH)。生成物氢化
2NaH)。生成物氢化
钠的电子式为_________,含有的化学键为_______键(填“离 子”、“共价”或“金属”)。
子”、“共价”或“金属”)。
(3)元素周期表中元素的性质存在递变规律,下列比较正确的是________。
a.碱性:NaOH>Mg(OH)2>Al(OH)3b.酸性:H4SiO4>H3PO4>H2SO4>HClO4
c.氢化物稳定性:PH3<H2S<HCl d.与NaOH溶液反应的剧烈程度:Na>Mg>Al
(4)第三周期元素的气态原子失去最外层一个电子所需能量(设为E)如图所示: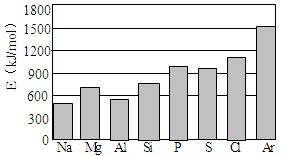
① 同周期内,随着原子序数的增大,E值变化的总趋势是________________。
② 根据上图提供的信息,试推断E氟_______E氧(填“>”“<”或“=”)。
下图中 A、B、C、D、E均为有机化合物。已知:C能跟NaHCO3发生反应,C和D的相对分子质量相等,且E为无支链的化合物。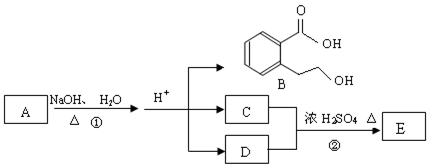
根据上图回答问题:
(1)已知E的相对分子质量为102,其中碳、氢两种元素的质量分数分别为58.8%、9.8%,其余为氧,则E的分子式为; C分子中的官能团名称是 ______________;化合物B不能发生的反应是(填字母序号):
a.加成反应 b.取代反应 c.消去反应 d.酯化反应 e.水解反应 f. 置换反应
(2)反应②的化学方程式是__________________。
(3)反应②实验中加热的目的是:
Ⅰ。;
Ⅱ。。
(4)A的结构简式是 ________ __________。
__________。
(5)同时符合下列三个条件的B的同分异构体的数目有个。
Ⅰ.含有间二取代苯环结构 Ⅱ.属于非芳香酸酯 Ⅲ.与 FeCl3溶液发生显 色反应。写出其中任意一个同分异构体的结构简式。
色反应。写出其中任意一个同分异构体的结构简式。
某兴趣小组为验证日常生活用的火柴头上含有KClO3、MnO2、S,设计了以下实验流程图:
(1)为了验证气体A,按右图所示进行实验:若能观察到现象,即可证明火柴头上含有S元素。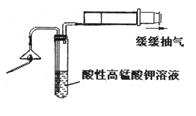
(2)步骤①中发生的与此相 关的两个主要反应的方程式是,
关的两个主要反应的方程式是,
。
(3)步骤②所用玻璃仪器的名称是。
(4)要证明火柴头中含有氯元素的后续实验步骤是
。
(5)有学生提出了检验火柴头上氯酸钾的另一套可行的实验方案:
则有关反应的离子方程式为。
某工业废水中仅含下表离子中的5种(不考虑水的电离及离子的水解),且各种离子的物质的量浓度相等,均为0.1mol/L。
| 阳离子 |
K+ Cu2+ Fe3+ Al3+ Ag+ |
| 阴离子 |
I-CO32- NO3- SO42- SiO32- |
甲同学欲探究废水的组成,进行了如下实验:
Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,呈紫色火焰(透过蓝色钴玻璃观察)。
Ⅱ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清。
Ⅲ.另取溶液加入BaCl2溶液,有白色沉淀生成,加稀硝酸沉淀无变化。
请推断:
(1)由Ⅰ判断,溶液中一定含有的阳离子是(写离子符号)。
(2)Fe3+是否存在?,判断的理由是
。
(3)Ⅲ中加入少量盐酸生成无色气体的的离子方程式是_________________________。
将Ⅲ中所得红棕色气体通入水中,气体变无色,所发生的化学方程式为
_______________________________________________________________
(4)甲同学最终确定原溶液中所含阳离子是 ,阴离子是。(写离子符号)
,阴离子是。(写离子符号)
(5)另取100mL原溶液,加入足量的氨水,充分反应后过滤,洗涤,灼烧至恒重,得到的固体质量为 g。
g。