为证明某可溶性一元酸(HX)是弱酸,有如下实验方案,其中不合理的是
| A.室温下,测0.1 mol/L HX溶液的pH,若pH>1,证明HX是弱酸 |
| B.室温下,测1 mol/L NaX溶液的pH,若pH>7,证明HX是弱酸 |
| C.相同条件下,对0.1 mol/L的HCl和0.1 mol/L的HX进行导电性实验,若与HX溶液相串联的灯泡较暗,证明HX为弱酸 |
| D.将等浓度、等体积的HCl和NaX溶液混合,若混合溶液pH<7,证明HX是弱酸 |
X、Y、Z三种短周期元素,原子半径的大小关系为: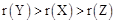 ,原子序数之和为16。X、Y、Z三种元素的常见单质在适当条件下可发生下图所示变化,其中B和C均为10电子分子。下列说法不正确的是()
,原子序数之和为16。X、Y、Z三种元素的常见单质在适当条件下可发生下图所示变化,其中B和C均为10电子分子。下列说法不正确的是()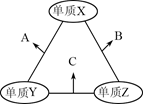
| A.X元素位于ⅥA |
| B.A不能溶解于B中 |
| C.B的沸点高于C的沸点 |
| D.A和C不可能发生氧化还原反应 |
下列叙述正确的是()
| A.相同数目的H318O+和D2O分子中的中子数相等 |
| B.54 24Cr为铬的一种核素,其核外电子数为30 |
| C.标准状况下,22.4L氦气与22.4L氟气所含原子数均为1.204×1024 |
| D.Na2O2与H2O反应生成氧气,反应中水作还原剂 |
近期陆续曝光了一些制药企业为了谋求暴利,用经生石灰处理过的皮革废料,熬制成工业明胶,制成药用胶囊。下列说法错误的是()
| A.工业明胶是一种从动物的结缔或表皮组织中的胶原部分水解出来的蛋白质,其制备过程中因混有杂质,经常显现出鲜艳的颜色,因此可以将其作为食品添加剂中的着色剂使用 |
| B.此次曝光出的毒胶囊中有大家熟悉的阿莫西林胶囊。阿莫西林是一种最常用的青霉素类广谱抗生素。病人在使用青霉素前一定要进行皮试 |
| C.皮革在工业加工时,要使用含铬的鞣制剂,因此往往会造成铬含量的严重超标。重金属铬可使人体内的蛋白质变性 |
| D.生石灰与水的反应产物俗称熟石灰,其在工业生产上有很多用途,如治理酸性废水、制取漂白粉等 |
常温下,Ag2SO4、AgCl、AgI的溶度积常数依次为:Ksp(Ag2SO4)=7.7×10-5、Ksp(AgCl)=1.8×10-10、Ksp(AgI)=8.3×10-17。下列有关说法中,错误的是( )
| A.常温下,Ag2SO4、AgCl、AgI在水中溶解能力依次减弱 |
| B.在AgCl饱和溶液中加入NaI固体,有AgI沉淀生成 |
| C.Ag2SO4、AgCl、AgI的溶度积常数之比等于它们饱和溶液的物质的量浓度之比 |
| D.在Ag2SO4饱和溶液中加入Na2SO4固体有Ag2SO4沉淀析出 |
实验测得常温下0.1mol/L某一元酸(HA)溶液的pH值等于1,0.1mol/L某一元碱(BOH)溶液里c(H+)/c(OH-)=10-12。将此两种溶液等体积混合后,所得溶液呈的各离子的浓度由大到小排列的顺序是()
A.c(B+)>c(A-)>c(OH-)>c(H+) B.c(A-)>c(B+)>c(H+)>c(OH-)
C.c(B+)=c(A-)>c(H+)=c(OH-) D.c(B+)>c(A-)>c(H+)>c(OH-)