(1)请回答下列问题:
①已知:①CO(g) + 1/2O2(g) = CO2(g) △H= -283.0kJ·mol-1
②CH3OH(l) + 3/2O2(g) = CO2(g)+2H2O(l) △H= -726.5kJ·mol-1
请写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:____________________________________________________________________;
②已知拆开1molH-H键、1molCl-Cl键、1molH—Cl键分别需要的能量是436kJ、243kJ、432kJ,则反应则反应:H2(g)+ Cl2(g)=2HCl (g) 的△H= 。
(2)已知25℃、101 kPa下,稀的强酸与稀的强碱溶液反应的中和热为 -57.3 kJ/mol。
①则表示稀硫酸与稀烧碱溶液中和反应的热化学方程式为: 。
②测定中和热实验时所需的玻璃仪器有烧杯、量筒、 、 。
某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:
(1)该反应的化学方程式为
(2)从开始至2min,Z的平均反应速率为
已知拆开1 mol H—H键、1 mol I—I、1 mol H—I键分别需要吸收的能量为436kJ、151k J、299k J。则由氢气和碘反应生成1 mol HI需要(填“放出”或“吸收”)k J的热量。
第三周期元素A、B、C,其原子序数依次增大,已知A的焰色为黄色,C的某种氧化物是形成酸雨的主要原因,且这三种元素的最高价氧化物的水化物有一种具有两性,且他们两两之间都能反应生成盐和水。
(1)填出元素符号A __________B __________C__________
(2) C 2- 离子结构示意图为
(3)A和C形成的化合物的电子式为,属于化合物。
完成下列问题
(1)羟基的电子式,二氧化碳的电子式,乙酸中官能团的名称丁烷同分异构体的结构简式
(2)苯和浓HNO3反应的化学方程式,反应类型为.
下列共有十二种化学符号:
①O2②614C③238U④1123Na⑤O3⑥714N⑦1224Mg⑧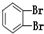
⑨235U⑩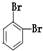 (11)
(11)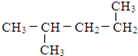 (12)
(12)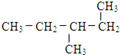
其中:
(1)表示核素的符号共有___种.
(2)互为同位素的是___(填序号,以下相同)
(3)质量数相等,但不能互称同位素的是__
(4)中子数相等,但质子数不相等的是___.
(5)互为同素异形体的是___.
(6)互为同分异构体的是___.