下列对化学平衡移动的分析中,不正确的是
①已达平衡的反应C(s)+H2O(g) CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动
CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动
②已达平衡的反应N2(g)+3H2(g) 2NH3(g),当增大N2的浓度时,平衡向正反应方向移动,N2的转化率一定升高
2NH3(g),当增大N2的浓度时,平衡向正反应方向移动,N2的转化率一定升高
③有气体参加的反应平衡时,若减小反应器容积时,平衡一定向气体体积增大的方向移动
④有气体参加的反应达平衡时,在恒压反应器中充入稀有气体,平衡一定不移动
| A.①④ | B.①②③ | C.②③④ | D.①②③④ |
下列关于有机化合物的说法正确的是()
| A.乙醇和乙酸中一定共面的原子数相等 |
| B.高锰酸钾可以氧化苯和甲烷 |
| C.甲烷和乙烯都可以与氯气反应 |
| D.乙烯可以与氢气发生加成反应,苯不能与氢气加成 |
2007年12月4日浙江省卫生厅公布的最常见的四种疾病中,高血压排在第一位,胆结石排在第二位,可见在全民社会中普及如何预防胆结石显得尤为重要。从化学上讲,非结合胆红素(VCB)分子有羟基,被氧化后(生成羧基)与钙离子结合形成胆红素钙的反应,就是一个生成沉淀的离子反应,从动态平衡的角度分析能预防胆结石的方法是()
A.大量食用纯碱可使钙离子沉淀完全,预防胆结石产生
B.不食用含钙的食品
C.适量服用维生素E、维生素C等抗氧化自由基可预防胆结石
D.手术切除胆囊
【2009年大连市高三年级双基考试】下列实验能获得成功的是()

A.无水乙酸和乙醇共热制取乙酸乙酯 |
B.乙烯和乙烷都能使溴的四氯化碳溶液褪色 |
C.将铜丝在酒精灯上加热后,立即伸人无水乙醇中,铜丝恢复原来的红色 |
D.淀粉用酸催化水解后的溶液加入新制银氨溶液,水浴加热,可看到有银镜出现 |
【2009年大连市高三年级双基考试】下列说法正确的是【】
A.在有机物分子中,含有的氢原子个数一定是偶数 |
B.分子组成相差若干个CH2的有机物互为同系物 |
C.所有糖类物质都有甜味 |
D.油脂是食物中产生能量最高的营养物质 |
(08海南模拟)被誉为中国“新四大发明”的复方蒿甲醚是第一个由中国发现的全新化学结构的药品,也是目前在国际上获得广泛认可的中国原创药品。截至2005年底,已被26个亚非国家指定为疟疾治疗一线用药,它在疟疾这一高传染性疾病治疗史上具有里程碑意义。其主要成分是青蒿素(是一种由青蒿中分离得到的具有新型化学结构的抗疟药),结构如下图所示。有关该化合物的叙述正确的是()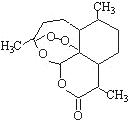
| A.分子式为:C16H22O5 |
| B.该化合物在一定条件下不能与NaOH溶液反应 |
| C.该化合物中含有过氧键,一定条件下有氧化性 |
| D.青蒿素与维生素一样是水溶性的 |