下列化学方程式中,能用离子方程式:Ba2++SO42-=BaSO4↓表示的是
| A.Ba(OH)2+(NH4)2SO4=BaSO4↓+2NH3•H2O |
| B.Ba(OH)2+H2SO4=BaSO4↓+2H2O |
| C.BaCO3+H2SO4=BaSO4↓+2H2O+CO2↑ |
| D.BaCl2+ Na2SO4=BaSO4↓+2NaCl |
如图集气瓶中用滤纸折成的纸蝴蝶上喷洒了一种溶液,通入某种气体后,实验结果与预测的纸蝴蝶颜色变化不一致的是( )
| A |
B |
C |
D |
|
| 喷洒液 |
酚酞 |
紫色石蕊 |
酸性重铬酸钾 |
酸化的KI—淀粉 |
| 通入的气体 |
NH3 |
Cl2 |
CH3CH2OH(g) |
O3 |
| 预测的颜色变化 |
变为红色 |
最终褪色 |
无明显变化 |
变为蓝色 |
某未知溶液中已检验出含大量的Fe2+、SO42—,且pH=1。欲检验此溶液中是否大量存在以下离子:①NH4+、② SiO32—、③Mg2+、④Cl-、⑤Ca2+、⑥ClO-,其中不需要检验就可以否定的离子是( )
| A.①③⑤ | B.②⑤⑥ | C.①②⑥ | D.③④⑥ |
按以下实验方案可从海洋动物柄海鞘中提取具有抗肿瘤活性的天然产物。
下列说法错误的是( )
| A.步骤(1)需要过滤装置 | B.步骤(2)需要用到分液漏斗 |
| C.步骤(3)需要用到坩埚 | D.步骤(4)需要蒸馏装置 |
实验是化学研究的基础,关于下列各实验装置图的叙述中正确的是( )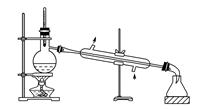
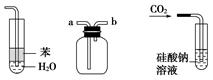
①② ③ ④
| A.装置①:常用于分离互不相溶的液体混合物 |
| B.装置②:可用于吸收NO2或HCl气体,并防止倒吸 |
| C.装置③:先从b口进气集满二氧化碳,再从a口进气,可收集一氧化氮 |
| D.装置④:可用来证明碳的非金属性比硅强 |
下列实验能达到目的的是( )
| A.用CCl4萃取碘水中的碘 |
| B.将足量盐酸加入混有少量CaCO3杂质的Na2SO4中可除去杂质 |
| C.将混有少量HCl的Cl2通入NaOH溶液中除去HCl |
| D.将Fe(OH)3固体加入沸水中制备Fe(OH)3胶体 |