根据以下三个热化学反应方程式:2H2S(g)+3O2(g) =2SO2(g)+2H2O(l) 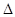 H= -Q1 kJ/mol;
H= -Q1 kJ/mol;
2H2S(g)+O2(g) =2S(s) +2H2O(l) 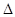 H= -Q2kJ/mol;
H= -Q2kJ/mol;
2H2S(g)+O2(g) =2S(s)+2H2O(g) 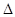 H= -Q3kJ/mol。
H= -Q3kJ/mol。
判断Q1、Q2、Q3三者关系正确的是
| A.Q1>Q2>Q3 | B.Q1>Q3>Q2 | C.Q3>Q2>Q1 | D.Q2>Q1>Q3 |
σ键可由两个原子的s轨道、一个原子的s轨道和另一个原子的p轨道以及一个原子的p轨道和另一个原子的p轨道以“头碰头”方式重叠而成。则下列分子中的σ键是由一个原子的s轨道和另一个原子的p轨道以“头碰头”方式重叠构建而成的是( )
| A.H2 | B.HCl | C.Cl2 | D.N2 |
将两个铂电极插入500mL CuSO4溶液中进行电解,通电一定时间后,某一电极增重0.064g(设电解时该电极无氢气析出,且不考虑水解和溶液体积变化),此时溶液中氢离子浓度约为
| A.4×10-3mol/L | B.2×10-3mol/L | C.1×10-3mol/L | D.1×10-7mol/L |
有三个烧杯,分别盛有氯化铜,氯化钾和硝酸银三种溶液;均以Pt作电极,将它们串联在一起电解一定时间,测得电极增重总和2.8克,这时产生的有色气体与无色气体的物质的量之比为
| A.4:1 | B.1:1 | C.4:3 | D.3:4 |
某碱性蓄电池在充电和放电时发生的反应为:
Fe+NiO2+2H2O Fe(OH)2+Ni(OH)2,下列说法中正确的是:
Fe(OH)2+Ni(OH)2,下列说法中正确的是:
| A.放电时,负极上发生反应的物质是Fe. |
| B.放电时,正极反应是:NiO2+2e-+2H+=Ni(OH)2 |
| C.充电时,阴极反应是:Ni(OH)2-2e-+2OH-=NiO2+2H2O |
| D.充电时,阳极附近pH值减小. |
N—H键能的含义是( )
| A.由N和H形成1 mol NH3所放出的热量 |
| B.把1 mol NH3的键全部拆开所吸收的热量 |
| C.拆开6.02×1023个N—H键所吸收的能量 |
| D.形成1个N—H键所放出的热量 |