课题式研究性学习是培养学生创造性思维的良好方法,某研究性学习小组将下列装置如图链接,C、D、E、F、X、Y都是惰性电极。将电源接通后,向乙中滴入酚酞试液,在F极附件先显红色。试回答下列问题: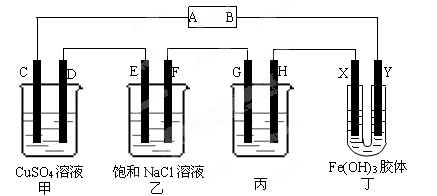
(1)电源A极的名称是 。
(2)甲装置中电解反应的总化学方程式: 。
(3)如果收集乙装置中产生的气体,相同状况下两种气体的体积比是 。
(4)欲用丙装置给铜镀银,G应该是 (填“铜”或“银”),电镀液的溶质是 (填化学式)。
(5)装置丁中的现象是 。
写出除去下列物质中杂质所选用的试剂,并用离子方程式表示:
(1)除去氯化钠溶液中的硫酸钠杂质,试剂 ,离子方程式 ;
(2)除去氧气中的二氧化碳杂质,试剂 ,离子方程式 ;
(3)除去铜中铁,试剂 ,离子方程式 。
(1)9.03×1023个二氧化碳的物质的量是 ,质量是 g。
(2)在100mL2mol/L硫酸溶液中,硫酸的质量是 g,氢离子的物质的量浓度为 mol/L
(3)“人造空气”(氧气O2与氦气He的混合气体)可用于减轻某病痛或供深水潜水员使用。在标准状况下,22.L“人造空气”的质量是9.6g,其中氧气与氦气的体积比为 ,氧气的质量是 g。
有下列物质:①二氧化碳②碳酸钙③氯气④醋酸⑤乙醇⑥石墨⑦氢氧化钠溶液⑧稀硫酸⑨熔融氯化钠⑩铝。请用序号回答下列问题:
(1)属于电解质的是 ,属于非电解质的是
(2)能够导电的是
(3)写出物质④的电离方程式
(1)在模拟溶洞的“形成”实验中,将过量二氧化碳气体通入饱和Ca(OH)2溶液中,产生CaCO3白色沉淀的质量与通入的二氧化碳气体体积之间的关系曲线如图所示。试回答:
AB段曲线所表示的反应化学方程式是: 。
将B处生成的溶液煮沸,反应化学方程式是: 。
(2)已知硫可与热的KOH溶液发生反应,反应方程式如下:3S+6KOH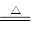 2K2S+K2SO3+3H2O
2K2S+K2SO3+3H2O
据此回答以下问题:
①在上述反应中,氧化剂与还原剂的物质的量之比为 。
②在上述反应中,若有3 mol硫单质参与反应,则转移电子的物质的量是 mol。
(1)一定温度下,有a.盐酸;b.硫酸;c.醋酸三种酸,用字母填写下列空格:
①当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是________________________。
②若三者c(H+)相同时,物质的量浓度由大到小的顺序是_________________________。
(2)常温下,0.1 mol·L-1的HCl溶液中,由水电离出来的H+浓度为________mol·L-1。
(3)在一元强碱MOH溶液中加入一元酸HA溶液,充分反应后,溶液呈中性。甲同学认为溶液中c(A-)=c(M+),而乙同学认为c(A-)和c(M+)是否相等,要看一元酸HA是强酸还是弱酸。你认为__________同学的说法正确,理由是____________________________。
(4)明矾[KAl(SO4)2·12H2O]常用作净水剂,其原理是_______________(用离子方程式表示)。
(5)将FeCl3溶液蒸干并灼烧,最终得到的固体物质是______________________(填写化学式)。