下列叙述正确的是
①7Li+中含有的中子数与电子数之比为2:1
②在C2H6分子中极性共价键与非极性共价键数之比为3:1
③常温下,11.2 L的甲烷气体中含有的氢、碳原子数之比为4:1
④5.6 g铁与足量的氯气反应失去的电子与参与反应的铁的物质的量之比为2:1
| A.①② | B.②③ | C.①③ | D.③④ |
铝是一种很重要的金属,可以发生一系列反应制备物质。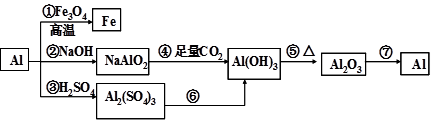
下列说法错误的是( )
| A.反应①又称铝热反应,曾用于野外焊接铁轨 |
| B.利用②③反应都能产生氢气,产生等量氢气消耗Al的质量也相等且转移电子数也相等 |
| C.常用反应⑥制备Al(OH)3,方法是向Al2(SO4)3溶液中滴加NaOH溶液至恰好完全沉淀 |
| D.工业上常用反应⑦制备金属铝,制备过程中常加入冰晶石以降低Al2O3的熔点 |
硅作为一种新型能源被广泛开发利用,关于其有利因素的下列说法中,你认为不正确的是( )
| A.硅燃烧产物对环境产生的污染,容易得到有效控制 |
| B.从Si(s)+O2(g)===SiO2(s) ΔH=-858.6 kJ·mol-1可知,硅燃烧放出的热量较多 |
| C.自然界中硅的贮存量丰富,可以从自然界直接获得单质硅 |
| D.硅便于运输、贮存,从安全角度考虑,硅是最佳的燃料之一 |
向含有Cu(NO3)2、Zn(NO3)2、Fe(NO3)3、AgNO3各0.1 mol 的混合溶液中加入0.1 mol铁粉,充分搅拌后,Fe溶解,溶液中不存在Fe3+,同时析出0.1 mol Ag。下列结论错误的是( )
| A.氧化性:Zn2+>Cu2+>Fe3+>Ag+ |
| B.Fe3+的氧化性大于Cu2+ |
| C.溶液中Cu2+与Fe2+的物质的量之比为1∶2 |
| D.1 mol Fe可还原2 mol Fe3+ |
有一块镁铝合金,其中镁与铝的质量比是8∶9。加入足量稀H2SO4使其完全溶解后,再加入NaOH溶液,生成沉淀的质量随NaOH溶液体积变化的曲线如下图,其中正确的是( )
有Fe2+、NO 、Fe3+、NH
、Fe3+、NH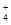 、H+和H2O六种微粒,分别属于一个氧化还原反应中的反应物和生成物,下列叙述错误的是( )
、H+和H2O六种微粒,分别属于一个氧化还原反应中的反应物和生成物,下列叙述错误的是( )
A.还原产物为NH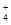 |
| B.氧化剂与还原剂的物质的量之比为8∶1 |
C.若有1 mol NO 作氧化剂,则转移8 mol e- 作氧化剂,则转移8 mol e- |
| D.若把该反应设计为原电池,则负极反应为Fe2+-e-===Fe3+ |