已知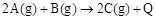 。下列说法或表达正确的是
。下列说法或表达正确的是
| A.使用催化剂可改变该反应的反应热 |
B. ; ;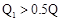 |
C.A和 混合气体的稳定性比C气体强 混合气体的稳定性比C气体强 |
| D.该条件下,2LC气体分解成2LA气体与1LB气体吸收的热量为Q |
甲~辛等元素在周期表中的相对位置如下表。甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素,下列判断正确的是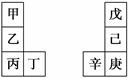
| A.丙与庚的原子序数相差3 |
| B.气态氢化物的热稳定性:戊>己>庚 |
| C.乙所在周期元素中,其简单离子的半径最大 |
| D.乙的单质在空气中燃烧生成的化合物只含离子键 |
将少量SO2气体通入BaCl2和FeCl3的混合溶液中,溶液颜色由棕黄色变成浅绿色,同时有白色沉淀产生。针对上述变化,下列分析正确的是
| A.该实验表明SO2有漂白性 | B.白色沉淀为BaSO3 |
| C.该实验表明FeCl3有还原性 | D.反应后溶液酸性增强 |
下列有关能量的判断和表示方法正确的是
| A.由C(s,石墨)→C(s,金刚石)—1.9 kJ,可知:石墨比金刚石更稳定 |
| B.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量更多 |
| C.由H+(aq)+OH-(aq) →H2O(l)+ 57.3 kJ,可知:含1 mol CH3COOH的溶液与含1 mol NaOH的溶液混合,放出热量等于57.3 kJ |
| D.2 g H2完全燃烧生成液态水放出285.8 kJ热量,则氢气燃烧的热化学方程式为2H2(g)+O2(g) →2H2O(l)+285.8 kJ |
单位体积的稀溶液中,非挥发性溶质的分子或离子数越多,该溶液的沸点越高。下列溶液中沸点最高的是
| A.0.01 mol/L的蔗糖溶液 | B.0.02 mol/L的CH3COOH溶液 |
| C.0.02 mol/L的NaCl溶液 | D.0.01 mol/L的K2SO4溶液 |
钐(Sm)属于稀土元素,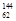 Sm与
Sm与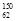 Sm是钐元素的两种同位素。以下说法正确的是
Sm是钐元素的两种同位素。以下说法正确的是
A.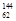 Sm与 Sm与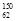 Sm互为同素异形体 Sm互为同素异形体 |
B.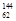 Sm与 Sm与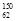 Sm具有相同核外电子排布 Sm具有相同核外电子排布 |
C.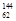 Sm与 Sm与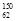 Sm的性质完全相同 Sm的性质完全相同 |
D.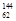 Sm与 Sm与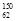 Sm的质子数不同,但中子数相同 Sm的质子数不同,但中子数相同 |