元素R、X、T、Z、Q在元素周期表中的相对位置如表所示,其中R单质在暗处与H2剧烈化合并发生爆炸。则下列判断正确的是
| A.非金属性:T<X <R |
| B.气态氢化物稳定性:R <T<Q |
| C.R与Q的电子数相差16 |
| D.X与Q最高价氧化物的水化物的质子数相差18 |
关于图中各装置的叙述不正确的是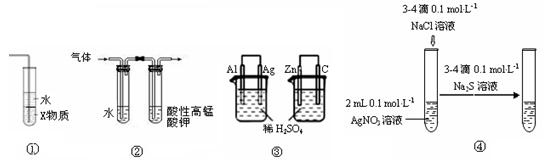
| A.装置①中X若为四氯化碳,可用于吸收氨气,并防止倒吸 |
| B.装置②可检验溴乙烷发生消去反应得到的气体中含有乙烯 |
| C.装置③的两个装置中通过导线的电子数相同时,消耗负极材料的物质的量不相同 |
| D.装置④能验证AgCl沉淀可转化为溶解度更小的Ag2S沉淀 |
下列实验或图表的结论或解释正确的是
| 实验或图表 |
结论或解释 |
|
| A |
铝 箔在酒精灯火焰上加热熔化但不滴落 箔在酒精灯火焰上加热熔化但不滴落 |
铝箔表面生成的氧化物具有高熔点 |
| B |
某CH3COOH和CH3COONa组成的酸性溶液中,加入一定量氨水 |
c(CH3COO-)一定大于c(Na+)、c(NH4+)之和 |
| C |
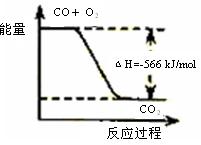 |
该反应热化学方程式为2CO(g)+O2(g)=2CO2(g)ΔH="-566" kJ/mol |
| D |
铁制容器可用于盛装冷的浓硫酸 |
铁与浓硫酸不反应 |
根据以下叙述制备氯化铜:先将浓盐酸用蒸气加热至80℃左右,慢慢加入含有FeO杂质的CuO粉,充分反应,使其溶解。已知:FeS不溶于水,但溶于酸;
| 溶液中被沉淀离子 |
Fe3+ |
Fe2+ |
Cu2+ |
| 完全生成氢氧化物沉淀时,溶液的pH |
≥3.7 |
≥9.6 |
≥6.4 |
在除去溶液中的Fe2+时,可采用的方法是
| A.可直接加碱,调整溶液的pH≥9.6 |
| B.加入纯铜粉,将Fe2+还原为Fe |
| C.先将Fe2+氧化成Fe3+,再调整溶液pH至3~4 |
| D.通入H2S使Fe2+直接沉淀 |
能正确解释下列反应原理的离子方程式
| A.AlCl3溶液中通入过量的NH3:Al3++4NH3·H2O=AlO2-+4NH4+ |
| B.淀粉碘化钾试纸上滴稀硝酸变蓝:2I- + 4H+ + NO3-= I2 + NO↑+ 2H2O |
C.电解MgCl2饱和溶液: MgCl2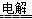 Mg+Cl2↑ Mg+Cl2↑ |
| D.用碳酸钠溶液浸泡锅炉水垢:CaSO4 + CO32- |
下列事实一定能说明HF是弱酸的是
①常温下NaF溶液的pH大于7; ②用HF溶液做导电性实验,灯泡很暗;
③HF与NaCl不能发生反应; ④常温下0.1mol/L的HF溶液的pH为2.3;
⑤HF能与Na2CO3溶液反应,产生CO2气体;⑥HF与水能以任意比混溶;
⑦1mol/L的HF水溶液能使紫色石蕊试液变红。
| A.①②⑦ | B.②③⑤ | C.③④⑥ | D.①④ |