在5.6 g Fe粉中加入过量的稀硫酸溶液,待反应完全后,再加入1mol·L-1 KNO3溶液25mL,恰好反应完全。该反应的方程式为:
FeSO4 +KNO3 +H2SO4→K2SO4 +Fe2(SO4)3+NxOy + H2O(未配平),则对该反应的下列说法正确的是
| A.化学方程式中按物质顺序的计量数是:8、2、5、1、4、1、5 |
| B.反应中氧化产物是N2O |
| C.反应过程中转移的电子数为8mol电子 |
| D.氧化产物和还原产物的物质的量之比为4∶1 |
若在铜片上镀银时,下列叙述正确的是
① 将铜片接在电池的正极上
② 将银片接在电源的正极上
③ 需用CuSO4溶液作电解液
④ 在银片上发生的反应是:4OH–- 4e–=O2↑+ 2H2O
⑤ 需用AgNO3溶液作电解液
⑥ 在铜片上发生的反应是:Ag+ + e-= Ag
| A.①③⑥ | B.②③④⑥ | C.①④⑤⑥ | D.②⑤⑥ |
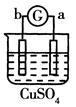
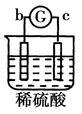
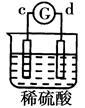
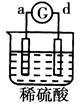
有a、b、c、d四个金属电极,G为电流计。有关的反应装置及部分反应现象如下:
| 实验 装置 |
 |
 |
 |
 |
| 部分实验现象 |
a极质量减小b极质量增加 |
溶液中的SO42-向b极移动 |
d极溶解c极有气体产生 |
电子从d极流向 a极 |
由此可判断这四种金属的活动性顺序是
A.d>a>b>c B. a>b>c>d C. b>c>d>a D. a>b>d>c
用惰性电极分别电解下列各物质的水溶液一段时间后,向剩余溶液中加入适量水能使溶液恢复到电解前浓度的是
| A.NaCl | B.H2SO4 | C.CuCl2 | D.AgNO3 |
如图所示装置中,观察到电流计指针偏转;M棒变粗;N棒变细,由此判断表中所列M,N,P物质,其中可以成立的是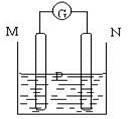
| M |
N |
P |
|
| A |
Zn |
Cu |
稀硫酸 |
| B |
Cu |
Fe |
稀盐酸 |
| C |
Ag |
Zn |
AgNO3溶液 |
| D |
Fe |
C |
CuSO4溶液 |
下列有关说法正确的是
| A.S(s,单斜)═S(s,正交) ΔH= +0.33kJ•mol‑1,正交硫比单斜硫稳定 |
| B.2H2(g)+O2(g)═2H2O(g); ΔH=﹣489.6kJ•mol-1,氢气的燃烧热为489.6kJ•mol-1 |
| C.当镀锌铁制品的镀层破损时,镀层仍能对铁制品起到保护作用 |
| D.锌锰干电池工作一段时间后碳棒变细 |