相同温度下,容积相同的甲、乙两个恒容密闭容器中均发生如下反应:2SO2(g) + O2(g)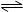 2SO3(g) + 197 kJ实验测得有关数据如下:
2SO3(g) + 197 kJ实验测得有关数据如下:
| 容器编号 |
起始时各物质的物质的量 / mol |
达到平衡时体系能量的变化/KJ |
||
| SO2 |
O2 |
SO3 |
||
| 甲 |
2 |
1 |
0 |
放出热量:Q1 |
| 乙 |
1.8 |
0.9 |
0.2 |
放出热量:Q2 |
下列判断中不正确的是
A.197>Q1>Q2
B.达到平衡时SO2的体积分数:甲>乙
C.两容器中反应的平衡常数相等
D.生成1molSO3(l)时放出的热量大于98.5kJ
用NA表示阿伏加德罗常数的值。下列判断正确的是
| A.18 g H2O含有的氢原子数目为NA |
| B.标准状况下,22.4 LCO2含有的分子数目为NA |
| C.1 L1mol·L-1K2SO4溶液中含有的钾离子数目为NA |
| D.1 mol H2在O2中完全燃烧转移的电子数目为NA |
下列反应的离子方程式书写正确的是
| A.盐酸与氢氧化钠溶液反应: H++OH-=H2O |
| B.锌粒与稀醋酸反应: Zn+2H+=Zn2++H2↑ |
| C.氯化镁溶液与氨水反应: Mg2++2OH-=Mg(OH)2↓ |
| D.氯气与氢氧化钠溶液反应: Cl2+OH-=Cl-+ClO-+H2O |
在含有大量K+、OH-、CO32-的溶液中还可能大量存在的离子是
| A.NH4+ | B.Al3+ | C.Ca2+ | D.SO42- |
下列各组原子序数所表示的两种元素,能形成AB2型离子化合物的是
| A. 6和8 | B.11和13 | C.11和16 | D.12和17 |
最高正化合价是它的负化合价的3倍的那一族元素是
| A.第ⅦA族 | B.第ⅥA族 | C.第ⅤA族 | D.第ⅢA族 |