请根据下图所示的实验过程和提供的数据(步骤②产生的气体全部逸出),回答下列问题:
(1)实验所用稀盐酸的溶质的质量分数为 .
(2)计算原混合物样品中CaCl2的质量(写出计算过程).
松油醇(C10H18O)是一种调香香精,多存在于松节油、芳樟油、玉树油、橙花油中,请回答:
(1)松油醇中碳元素、氢元素和氧元素三者的质量比是。
(2)多少克松油醇所含碳元素质量与30g葡萄糖(C6H12O6)所含碳元素质量相等。(请写出计算过程)
在实验室里加热30g氯酸钾(KClO3)和二氧化锰的混合物制取氧气,完全反应后剩余固体质量为20.4g。请计算:
(1)生成氧气的质量为g;(2)原混合物中氯酸钾的质量。
金属生锈会增加零件间的磨损,甚至造成火灾、爆炸等灾难性事故。某工厂为了减轻机械的锈蚀带来的损失,用盐酸(HCl)除铁锈(Fe2O3),已知发生反应的方程式为Fe2O3+6HCl=2FeCl3+3H2O,求:
若此次除铁锈结束后,生成了151.2g水,则此次除去铁锈的质量。
硫酸钾(K2SO4)是一种无氯、优质高效钾肥,特别是在烟草、葡萄、甜菜、马铃薯、亚麻及各种果树等忌氯作物的种植业中,是不可缺少的重要肥料。根据图所示的硫酸钾化肥的相关信息,求: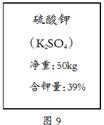
(1)K2SO4的相对分子质量。
(2)该化肥中含K2SO4的质量。
实验室常用氯酸钾与二氧化锰混合制取氧气.现将2.5g二氧化锰放入盛有氯酸钾的试管中加热,反应完全结束后,称量固体的质量减少了1.6g.请完成下列问题:
(1)反应结束后,收集到氧气的质量为g.
(2)计算加热前试管中氯酸钾的质量.