如图所示,这是一瓶用排水法收集好安放在桌面上的一瓶无色气体。据此请判断与这瓶气体相关的物理性质是:无色气体、_____________、______________。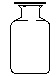
人通过肺与外界进行气体交换,吸入空气中的氧气,排出二氧化碳和水蒸气。为了验证吸入的气体与呼出的气体有什么不同,采用了下图装置进行实验。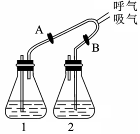
验证二氧化碳锥形瓶1和2中盛放的是________。连续数次吸气时,开关A和B的状态分别是________ (以“打开”或“关闭”进行说明);调整开关A和B,再进行连续数次呼气操作。整个过程中可观察到的现象是________,证明吸入和呼出气体中二氧化碳含量不同。
验证水蒸气更换锥形瓶1和2中的药品,连续进行吸气和呼气操作(步骤同上),为了得出正确的结论,还需要进行的操作是________。
根据下图回答问题。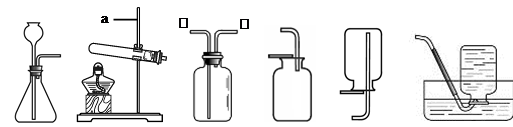
A B C D E F仪器a的名称为________。
实验室用高锰酸钾制取氧气:所选用的发生装置是________(填字母序号),反应的化学方程式为________。
实验室制取二氧化碳:选用的药品是________;选用的收集装置是________(填字母序号),用此装置收集,若证明气体是否收集满,应采取的操作是________。
金属在生产生活中应用广泛。以下用品中,主要利用金属导电性的是 ________(填字母序号)。



A.铝箔 B.铜导线 C.炒锅目前世界上每年因腐蚀而报废的金属设备和材料相当于年产量的20%~40%。钢铁锈蚀的条件是_________;盐酸常用于金属表面除锈,写出用盐酸清除铁锈(主要成分为Fe2O3)的化学方程式_________。
一般情况下,两种活动性不同的金属在潮湿的环境中接触时,活动性强的金属首先被腐蚀。造船工业为了避免轮船的钢铁外壳被腐蚀,通常在轮船外壳镶嵌的金属是_________(填字母序号)。
| A.银块 | B.铜块 | C.铅块 | D.锌块 |
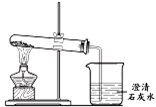
将木炭粉和氧化铁粉末的混合物加热(如图所示)一段时间,观察到澄清石灰水变浑浊;向反应后的固体中加入过量的稀盐酸,固体全部溶解且有气泡出现。根据现象判断,木炭和氧化铁反应的生成物中一定含有________;加盐酸后溶液中的溶质一定有________。
下列数据是氯化钠和氯化铵固体在不同温度时的溶解度。
| 温度/℃ |
0 |
20 |
40 |
60 |
80 |
100 |
| 溶解度/g NaCl |
35.7 |
36.0 |
36.6 |
37.6 |
38.4 |
39.8 |
| NH4Cl |
29.4 |
37.2 |
45.8 |
55.2 |
65.5 |
77.3 |
医疗上,氯化钠常用于配制0.9%的生理盐水,生理盐水中溶质为________。
从海水中提取食盐通常采取晾晒海水的方法,这是因为随温度升高氯化钠的溶解度变化 ________(填“大”或“小”)。
20℃时,向100 g水中加入25 g氯化钠,充分溶解后,溶液中溶质质量分数为 ________。
现有200 g溶质质量分数为10%的氯化钠溶液,若使溶液的溶质质量分数增加一
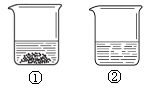
倍,应该蒸发掉 ________g水。30℃时,向两个分别盛有相同质量的氯化钠和氯化铵的烧杯中,各加入100 g水,充分溶解后,恢复至30℃,其结果如右图所示。有关下列说法中,正确的是________(填字母序号)。
| A.烧杯②中溶液是不饱和溶液 |
| B.升高温度或增加溶剂都有可能将烧杯①中固体全部溶解 |
| C.若将烧杯①中的溶液变为不饱和溶液,溶液中溶质质量分数一定减小 |
| D.将得到的烧杯②中溶液降温至0℃时,溶液中溶质质量分数一定减小 |
洁厕灵(有效成分为盐酸)、生石灰、小苏打、食盐都是日常生活中常用物质。洁厕灵不宜存放在铁制金属容器内,用化学方程式表示其原因________。
生石灰能够用于食品干燥剂,用化学方程式表示其干燥原理________。
小苏打在日常生活中常用于________(写出一种);小苏打和洁厕灵不能接触,用化学方程式表示其原因________。
氯化钠除食用外,还是一种重要的工业原料。例如可通过电解氯化钠溶液制取烧碱,同时生产氢气和氯气,写出该反应的化学方程式________。