下列有关物质应用的说法中,正确的是
| A.用石英器皿盛装氢氟酸 |
| B.臭氧具有强还原性,可用于自来水的杀菌消毒 |
| C.Fe3+具有氧化性,可腐蚀印刷线路板上的铜 |
| D.硫酸钡俗称“钡餐”,可用于治疗胃酸过多 |
实验室需配制一种仅含四种离子(不包括水电离出的离子)的混合溶液,且在混合液中四种离子的物质的量浓度均为0.5 mol/L,下面四个选项中能达到此目的的是( )
A.Fe2+、Na+、NO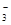 、Cl- 、Cl- |
B.Mg2+、NH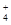 、SO 、SO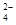 、NO 、NO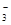 |
| C.H+、K+、Cl-、CH3COO- | D.Fe3+、K+、AlO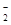 、SO 、SO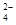 |
下列实验设计及其对应离子方程式均正确的是( )
| A.用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+===Cu2++2Fe2+ |
| B.Na2O2与H2O反应制备O2:Na2O2+H2O===2Na++2OH-+O2↑ |
| C.将氯气溶于水制备次氯酸:Cl2+H2O===2H++Cl-+ClO- |
D.用浓盐酸酸化的KMnO4与H2O2反应,证明H2O2具有还原性:2MnO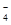 +6H++5H2O2===2Mn2++5O2↑+8H2O +6H++5H2O2===2Mn2++5O2↑+8H2O |
下列各溶液中一定能大量共存的离子组是( )
A.加入铝粉有氢气生成的溶液中:Mg2+、Cu2+、SO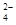 、K+ 、K+ |
B.使pH试纸呈红色的溶液中:Fe2+、I-、NO 、Cl- 、Cl- |
C.常温下,c(H+)=10-14mol/L的溶液中:Na+、AlO 、S2-、SO 、S2-、SO |
D.常温下,水电离出的c(H+)与c(OH-)乘积为10-28的溶液中:K+、Na+、HCO 、Ca2+ 、Ca2+ |
关于一些重要的化学概念有下列说法:①Fe(OH)3胶体和CuSO4溶液都是混合物;②BaSO4是一种难溶于水的强电解质;③冰醋酸、纯碱、小苏打分别属于酸、碱、盐;④煤的干馏、煤的汽化和液化都属于化学变化;⑤置换反应都属于离子反应。其中正确的是()。
| A.①②⑤ | B.①②④ | C.②③④ | D.③④⑤ |
下列有关物质结构的表述正确的是( )
A.次氯酸的电子式 |
B.二氧化硅的分子式SiO2 |
C.硫原子结构示意图 |
D.钠离子的结构示意图 |