水是最普通、最常见的物质之一。
(1)生活中的“水”有很多种。下列“水”属于纯净物的是 (填字母序号)。
| A.河水 | B.自来水 | C.蒸馏水 | D.矿泉水 |
(2)家用净水剂中通常使用 净水,这种物质既能吸附一些溶解在水中的杂质,又可粗略去除一些不溶性杂质。
(3)如图为电解水的装置,通电一段时间后,试管2中所收集的气体为 ,发生反应的化学方程式为 ,该反应属于 _(填“化合”或“分解”)反应。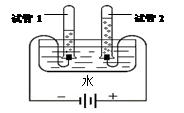
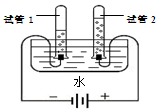
(4)水是一种重要的化工原料。氯碱工业通过电解饱和氯化钠溶液的方法制取烧碱(NaOH),同时还生成氢气和氯气(Cl2),其反应的化学方程式为 。
根据要求填空:
(1)熟石灰的化学式;
(2)在实验室可利用下图所示实验装置制取氧气。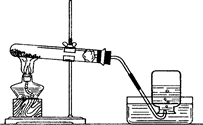
下图为粗盐的提纯过程,
(1)其中操作①、③依次为、;操作②玻璃棒的作用是。
(2)若NaCl的产率偏低( ),则可能的原因是(填字母)。
),则可能的原因是(填字母)。
A.过滤时滤纸有破损
B.蒸发时有固体溅出
C.溶解含泥沙的粗食盐时,加入的水量不足
(3)用上述实验所得NaCl晶体配制50g溶质质量分数为5%NaCl溶液,配制时需要的玻璃仪器有烧杯、玻璃棒、滴管、。
氨气易溶于水,易与浓硫酸反应,不与碱石灰(干燥剂)反应。氨气还具有还原性,在加热的条件下能将氧化铜还原为铜,同时生成氮气和水。反应的化学方程式为:2NH3 + 3CuO ="==" N2 + 3Cu + 3H2O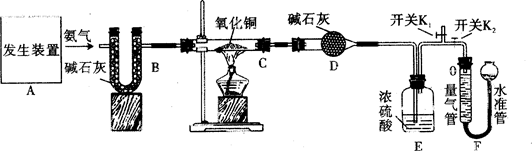
某化学小组为验证氨气的组成,设计了如下图所示实验。已知:该实验装置气密性良好,实验前装置C、D的质量分别为65.60 g、132.47 g,实验中所用试剂均足量。
实验步骤:
I.打开K1,关闭K2,通人氨气一段时间后,关闭K1,打开K2。(注:K1接个气球)
Ⅱ.点燃酒精灯加热,待黑色固体部分变为红色后,停止加热。
Ⅲ.继续通氨气至玻璃管冷却。
Ⅳ.记录量气管读数为VmL。
V.称量装置C、D的质量分别为65.36 g、132.74 g。
请回答下列问题:
(1)若用加热氯化铵和熟石灰固体制取氨气,则发生装置与实验室制取二氧化碳气体装置(填“相同”或“不相同”)。
(2)步骤Ⅳ读数时,应注意视线、刻度线。三线在一条直线上。
(3)反应生成水的质量为。
(4)实验过程中通入氨气的作用各不相同。步骤I是;步骤Ⅱ是还原氧化铜;步骤Ⅲ是。
(5)请根据该实验数据列计算式,证明氨气中不含氧元素。相关计算式为。
为了探究二氧化碳的性质,及证明石灰石是碳酸盐。某同学设计了如图所示的实验:
(1)写出石灰石与稀盐酸反应的化学方程式:。
(2)用注射器注入稀盐酸,一段时间后,可观察到在1、2两处中有一处有明显的现象发生,该实验现象是。
(3)当观察到,。(填现象)证明石灰石是碳酸盐,
(4分)化学是一门以实验为基础的科学。根据如图所示实验,回答以下问题。
①A为测定空气中氧气含量的实验装置,加入足量红磷的原因是,通过该实验可得出氧气约占空气总体积的的结论。
②集气瓶B中的现象:铁丝在氧气中剧烈燃烧,,放出大量的热。
③现在有氢气、甲烷、氧气,其中C中可能装的气体的化学式是。