某同学设计如图所示的实验装置,进行一氧化碳还原氧化铜的实验。试回答: 
(1)该装置存在的一个主要问题,对此你的改进方法是 .
(2)实验开始时,先通入一氧化碳,再给氧化铜加热,,原因是 ,
(3)实验过程中,图中A处能观察到的实验现象是 。 发生反应的化学方程式为 。
海水是一种重要的自然资源。以下是我市对海水资源的部分利用。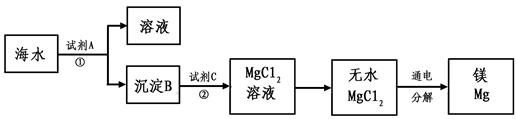
(1)从海水中获取淡水。常用的操作方法是 。
(2)从海水中获得氯化钠。将海水进行可得到粗盐;为除去粗盐中含有
的SO42-、Ca2+、Mg2+等杂质,-有如下操作:①溶解;②加过量的Na2CO3溶液; ③加过量的BaCl2溶液;④加适量的盐酸;⑤加过量NaOH溶液;⑥蒸发结晶;⑦过滤。正确的操作顺序是 。(用序号填一种合理组合)。
(3)从海水中得到金属镁。下图是从海水中提取镁的简单流程。
上述过程中,沉淀B与试剂C发生的是中和反应,则沉淀B的化学式为 ,由无水MgCl2制取Mg的化学方程式为 。海水本身就是含有MgCl2的溶液,它与通过步骤①、②得到的MgCl2溶液有何不同:
。
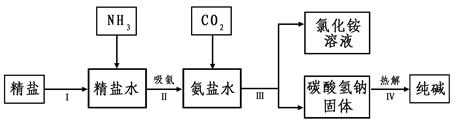
(4)海水“制碱”。下图是海水“制碱”的部分简单流程。
步骤Ⅲ、步骤Ⅳ反应的化学方程式为: 、
。
制氨盐水的过程中要先通入氨气,再通入二氧化碳。如果反过来,二氧化碳的吸收率会降低。这是因为 。
海水经过晒盐后得到粗盐和苦卤,重结晶后的食盐中还含有硫酸钠、氯化镁、氯化钙等可溶性杂质,他们在溶液中主要以SO42-、Ca2+、Mg2+的形式存在,为将这些杂质离子除净,应加入过量的氯化钡、氢氧化钠、碳酸钠等物质将其转化为沉淀,过滤除去;再加入适量的盐酸,得到精盐水,最后经蒸发即得精盐。以下是某化工厂对海水进行综合利用的示意图:
(1)在苦卤制镁的过程中加入了石灰乳(主要成分是氢氧化钙),石灰乳是用生石灰制得的,请写出制取石灰乳的化学方程式_________________________________________。
(2)在制备精盐的过程中,氯化钡和碳酸钠溶液的添加顺序是否可以颠倒________,理由是_____________________________________________________________________;
(3)在利用粗盐制备精盐过程的第⑥步操作中,加入适量盐酸的目的是__________
____________________________________________________________________。
酸、碱、盐是有广泛用途的重要化合物。某化学活动小组的同学围绕这几类化合物进行了一系列的探究活动。
(1)同学们打开盛浓盐酸和浓硫酸试剂瓶的瓶盖,立即就能把它们区分开来,这是为什么?
(2)右图是某试剂瓶标签上的内容。要把10g这种浓硫酸稀释为20%的硫酸,需要水的质量为g。稀释浓硫酸时,不可将水倒进浓硫酸里,请解释其原因。
(3)为探究一瓶氢氧化钠固体的变质情况,同学们进行了如下实验。全品中考网
①取少量该固体样品置于试管中,向其中加入一种无色溶液,发现有气泡产生,说明该样品中含有碳酸钠,由此可确定该固体已发生变质。则无色溶液可能是。
②为探究该固体中是否还有未变质的氢氧化钠,同学们又进行了如下表所示的实验。已知碳酸钠的水溶液呈碱性,它的存在会对氢氧化钠的检验造成干扰。请根据右图部分物质的溶解性表(20℃)所提供的信息,将下表填写完整。
| 实验目的 |
实验操作 |
现象 |
结论或化学方程式 |
除去碳酸钠 |
取少量该固体样品溶于水配成溶液,滴加适量的溶液, 充分反应后过滤 |
有白色沉淀生成 |
有关反应的化学方程式为 |
| 检验是否含有氢氧化钠 |
在滤液中滴加酚酞溶液 |
该样品中含有氢氧化钠 |
(4)若73g质量分数为20%的盐酸与127g氢氧化钠溶液恰好完全中和,试计算反应后所得溶液中溶质的质量分数。
右下图标出的是有关热水瓶的组成物质,请回答下列问题。
⑴所标物质中为金属材料的是(写一种即可),为有机合成材料的是。
⑵使用几天后,瓶胆内壁有水垢出现,这是因为水的硬度较大的缘故。请你写出一种鉴别硬水与软水的方法:。
⑶可用厨房中的一种常用物质(写名称)除去瓶胆内壁的水垢(已知水垢的主要成分是CaCO3)。
大龙在公园看到绿化工人往树干上涂抹具有杀菌杀虫作用的悬浊液,对其成份产生了好奇,于是他带回了一些样本进行研究.
信息提示:许多金属或它们的化合物在灼烧时都会使火焰呈现特殊的颜色,这叫做焰色反应.如:钠﹣﹣黄色;钙﹣﹣砖红色;钾﹣﹣紫色;钡﹣﹣黄绿色
Ⅰ猜想与假设:该制剂可能为波尔多液
Ⅱ实验探究:
| 序号 |
实验步骤 |
实验现象 |
| ① |
取样,将其置于大试管中,加入一定量水,静置片刻 |
上层有黄色固体漂浮,中层为无色液体,下层有较多白色固体 |
| ② |
取少量中层液体滴加无色酚酞试液 |
无色酚酞试液变红 |
| ③ |
另取少量中层液体进行焰色反应 |
火焰呈现砖红色 |
| ④ |
取少量黄色固体灼烧 |
燃烧,放热,产生淡蓝色火焰,有刺激性气味 |
| ⑤ |
向下层白色固体中滴加足量稀盐酸 |
固体完全溶解,但仅产生少量气泡 |
Ⅲ实验结论:
(1)根据上述实验①,可以判断该悬浊液中 (填“含”或“不含”)硫酸铜;
(2)根据上述实验 (填序号),可以判断该悬浊液中含有氢氧化钙;
(3)根据上述实验④,可以判断黄色固体是 ;
(4)写出⑤中发生的所有反应的化学方程式: .