Cl2是纺织工业中常用的漂白剂,Na2S2O3可作为漂白布匹后的“脱氯剂”。S2O32-和Cl2反应的产物之一为SO42-。下列说法中,不正确的是
| A.该反应中氧化剂是Cl2 |
| B.根据该反应可判断还原性:S2O32- > Cl- |
| C.上述反应中,每生成l mol SO42-,转移4 mol电子 |
| D.SO2与氯气的漂白原理相同,所以也可以用SO2做纺织工业的漂白剂 |
海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程。下列有关说法正确的是
| A.制取NaHCO3的反应是利用其溶解度小于NaCl |
| B.用澄清的石灰水可鉴别NaHCO3和Na2CO3 |
| C.在第③、④、⑤步骤中,溴元素均被氧化 |
| D.工业上通过电解饱和MgCl2溶液制取金属镁 |
对于实验I〜IV的描述正确的是

| A.实验I:逐滴滴加稀盐酸时,试管中立即产生大量气泡 |
| B.实验II:充分振荡后静置,下层溶液为橙红色,上层无色 |
| C.实验III:从饱和食盐水中提取NaCl晶体 |
| D.装置IV:酸性KMnO4溶液中有气泡出现,且溶液颜色逐渐变浅乃至褪去 |
能正确表示下列反应的离子方程式是
| A.Fe2O3溶于过量氢碘酸溶液中:Fe2O3 + 6H+ + 2I-=2Fe2+ + I2 +3H2O |
| B.铝粉与NaOH溶液反应:2Al + 2OH-=2AlO2-+ H2↑ |
| C.5.6 g Fe与200 mL 2.0 mol/L HNO3溶液充分反应:3Fe + 2NO3-+ 8H+=3Fe2+ + 2NO↑ + 4H2O |
D.碳酸氢铵溶液与足量的NaOH溶液混合后加热:NH4++OH- NH3↑+H2O NH3↑+H2O |
设NA为阿伏加德罗常数的值。下列说法正确的是
| A.标准状况下,22.4 L CCl4含有C-Cl键的数目为4 NA |
| B.常温常压下,44 g 由N2O与CO2组成的混合气体含有的氧原子数目为NA |
C.反应NH4N3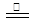 2N2↑+ 2H2↑,常温常压下每生成22.4 L N2,转移电子的数目为2 NA 2N2↑+ 2H2↑,常温常压下每生成22.4 L N2,转移电子的数目为2 NA |
| D.1 L 1 mol·L-1的AlCl3溶液中含有Cl-的数目为3NA |
下列化学用语使用正确的是
A.Mg2+结构示意图: |
B.质子数为92,中子数为146的U原子: |
C.NH4Cl的电子式: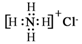 |
D.四氯化碳分子球棍模型:  |