氨有着广泛的用途,可用于化肥、硝酸、合成纤维等工业生产。
(1)根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应可生成氨气:
该反应在固定体积的密闭容器中进行,有关说法正确的是_____________(填序号字母)。
A.反应处于平衡状态时,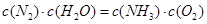 |
B.反应达到平衡后, |
| C.体系的总压强不变,说明反应已达平衡 |
| D.混合气体的密度保持不变,说明反应已达平衡 |
(2)液氨作为一种潜在的清洁汽车燃料已越来越被研究人员重视。它在安全性、价格等方面较化石燃料和氢燃料有着较大的优势。氨在燃烧试验机中相关的反应有: ①
① ②
② ③
③
请写出上述三个反应中 、
、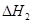 、
、 三者之间关系的表达式,
三者之间关系的表达式, =_________。
=_________。
(3)工业制硝酸的主要反应是:
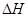 =
=
①升高温度,反应的K值减小,则Q______(填“>”、“<”或“=”)0。
②若反应起始的物质的量相同,下列关系图错误的是________(填序号)。

③在容积固定的密闭容器中发生上述反应,容器内部分物质的浓度如下表:
| 时间/浓度 |
  |
  |
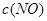  |
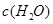  |
| 起始 |
4.0 |
5.5 |
0 |
0 |
| 第2min |
3.2 |
a |
0.8 |
1.2 |
| 第4min |
2.0 |
3.0 |
2.0 |
3.0 |
| 第6min |
2.0 |
3.0 |
2.0 |
3.0 |
反应在第2 min到第4 min时,O2的平均反应速率为________。
反应在第2 min时改变了条件,改变的条件可能是______________________________。
该条件下,反应的平衡常数K=________。
(本题共8分)
白磷(P4)是一种常见的晶体,可用于制备较纯的磷酸。根据题意回答:
1.31g白磷与足量的氧气完全燃烧生成P2O5固体,释放出745.5 kJ的热量,请写出白磷燃烧的热化学反应方程式:;
2.完成并配平白磷和氯酸溶液反应的化学方程式:
P4 + HClO3 + → HCl + H3PO4
3.白磷有毒,在实验室可采用CuSO4溶液进行处理,其反应为:
11P4 + 60CuSO4 + 96H2O → 20Cu3P + 24H3PO4 + 60H2SO4
该反应的氧化产物是,若有1.1 mol P4反应,则有mol电子转移。
4.磷的一种化合物叫亚磷酸(H3PO3)。已知:⑴0.1 mol/L H3PO3溶液的pH = 1.7;⑵H3PO3与NaOH反应只生成Na2HPO3和NaH2PO3两种盐;⑶H3PO3和碘水反应,碘水棕黄色褪去,再加AgNO3有黄色沉淀生成。关于H3PO3的说法:①强酸;②弱酸;③二元酸;④三元酸;⑤氧化性酸;⑥还原性酸,其中正确的是.
| A.②④⑥ | B.②③⑥ | C.①④⑤ | D.②③⑤ |
用于金属焊接的某种焊条,其药皮由大理石、硅酸盐、硅铁等配制而成。根据题意回答:
1.Al原子的核外电子排布式为_____________________;Al与NaOH溶液反应的离子方程式为________________________________________________。
2.Si原子核外有种不同能量的电子。硅铁属于合金,它的熔点比纯铁
(填“高”、“低”或“不一定”)。
3.Al3+与Yn-的电子数相同,Y所在族的各元素的氢化物的水溶液均显酸性,则该族氢化物中沸点最低的是________,最不稳定的是。
4.焊接过程中,药皮在高温下产生了熔渣和一种气体,该气体是_________,该气体在固态时属于晶体。
下表为元素周期表中的一部分,表中列出了11种元素在周期表中的位置,按要求完成下列各小题。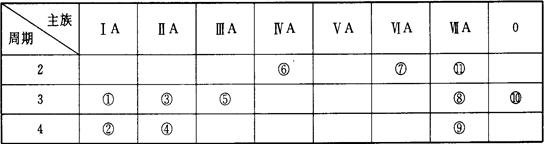
(1)化学性质最不活泼的元素是(填元素符号或化学式,下同),
非金属性最强的元素是。
金属性最强的单质与水反应的离子方程式是
。
(2)①③⑤三种元素的最高价氧化物对应的水化物中,碱性最强的化合物的化学式是
(3)①②③三种元素的原子半径由大到小的顺序是>>。
(4)某元素的最高价氧化物对应的水化物既能与酸反应生成盐和水,又能和碱反应
生成盐和水,该元素的最高价氧化物和盐酸反应的离子方程式为
。
向该元素和⑧号元素形成的化合物的溶液中,缓慢滴加氨水至过量,产生的实验现象是,有关反应的化学方程式为。(5)⑥元素形成的单质与浓硝酸发生化学反应的化学方程式为
。
现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。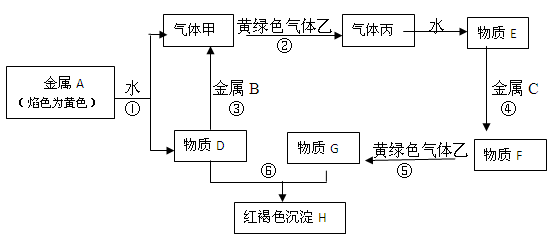
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:A、B、C
甲、乙、H
(2)写出下列反应的离子方程式:
反应⑤
反应⑥
(12分)配平下列各氧化还原反应方程式(将系数填写在相应横线上,并按要求填空)
⑴ ___ KMnO4+ ___ HCl =" _____" MnCl2+ _____ KCl + ____ Cl2 ↑ + ___ H2O
⑵_____ HNO3 = ___NO2 ↑ + _____ O2 ↑+ _____H2O
配平如下反应方程式并标注电子转移的方向和数目
⑶_____Na +____Cu2+ + ____H2O ==______Na+ + ____Cu(OH)2 ↓ + ____H2 ↑
该反应的氧化剂是;若转移的电子数是1mol,得到H2mol