某溶液中可能含有H+、NH4+、Mg2+、Fe3+、Al3+、SO42-、HCO3—等离子。当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随加入NaOH溶液的体积变化如图所示,下列说法正确的是
| A.d点溶液中含有的溶质只有Na2SO4 |
| B.原溶液中含有的Fe3+和Al3+的物质的量之比为1:1 |
| C.ab段发生的离子反应为:Al3++3OH-= Al(OH)3↓,Mg2++2OH—= Mg(OH)2↓ |
| D.原溶液中含有的阳离子必定有H+、NH4+、Al3+,但不能肯定Mg2+和Fe3+中的哪一种 |
某元素离子Am-的核内有n个中子,核外有x个电子。该元素原子的质量数为( )
| A.x-n+m | B.x+m+n | C.m+n-x | D.x-m+n |
有三种金属元素a、b、c,在相同条件下,b的最高价氧化物的水化物的碱性比a的最高价氧化物的水化物的碱性强;a可以从c的盐溶液中置换出c。则这三种金属元素的金属性由强到弱的顺序是( )
| A.a、b、c | B.b、a、c |
| C.b、c、a | D.c、b、a |
下列气态氢化物中,最稳定的是( )
| A.NH3 | B.PH3 | C.CH4 | D.H2 O |
短周期金属元素甲~戊在周期表中的相对位置如右表所示,下面判断不正确的是( )
| 甲 |
乙 |
|
| 丙 |
丁 |
戊 |
A、原子半径:丙>丁>戊 B、金属性:甲<丙
C、最外层电子数:甲>乙 D、氢氧化物碱性:丙>丁>戊
下列属于同位素的一组是( )
A、O2、O3 B、Na2O、Na2O2 C、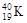 、
、 D、H、D、T
D、H、D、T