“嫦娥一号”卫星完成四大科学目标之一是探测下列14种元素的含量和分布:K、Th(钍)、U(铀)、O、Si、Mg、Al、Ca、Fe、Ti(钛)、Na、Mn、Cr(铬)、Gd(钆),其原子的最外层电子数是奇数的主族元素有
| A.2种 | B.3种 | C.4种 | D.5种 |
化学与社会可持续发展密切相关。下列做法不合理的是
| A.CO2合成可降解的聚碳酸酯类塑料,实现“碳循环” |
| B.提倡步行、骑自行车、乘公交车等“低碳”出行方式 |
| C.将废电池深埋,防止重金属污染 |
| D.开发利用各种新能源,减少对化石燃料的依赖,可以降低空气中PM2.5的含量 |
做实验时不小心使皮肤上沾了一些高锰酸钾,形成的黑斑很久才能消除,如果用草酸(H2C2O4乙二酸)的稀溶液洗涤,黑斑可以迅速褪去,其离子方程式为:
MnO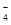 + C2O
+ C2O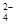 + H+ === CO2↑ + Mn2+ +
+ H+ === CO2↑ + Mn2+ +
下列有关叙述不正确的是
| A.该反应的氧化剂为KMnO4 |
B.发生还原反应的是C2O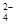 |
| C.该离子方程式右侧方框内的产物是H2O |
| D.16mol H+参加反应时,电子转移10 mol |
已知下列反应:Co2O3+6HCl(浓)===2CoCl2+Cl2↑+3H2O(Ⅰ);
5Cl2+I2+6H2O===10HCl+2HIO3(Ⅱ)。下列说法正确的是
| A.还原性:CoCl2>HCl>I2 |
| B.氧化性:Co2O3>Cl2>HIO3 |
| C.反应Ⅰ中HCl是氧化剂 |
| D.反应Ⅱ中Cl2发生氧化反应 |
下列离子反应方程式表示正确的是
| A.过量石灰水与碳酸氢钙反应:Ca2++2HCO3-+2OH-===CaCO3↓+CO32-+2H2O |
| B.FeSO4酸性溶液暴露在空气中:4Fe2++O2+4H+===4Fe3++2H2O |
| C.向氯化铝溶液中滴加过量氨水:Al3++4NH3·H2O===AlO2-+4NH4++2H2O |
| D.H2SO4与Ba(OH)2溶液反应:Ba2++OH-+H++SO42-===BaSO4↓+H2O |