有一种MCFC型燃料电池,该电池所用燃料为H2和空气,电解质为熔融的K2CO3。电池的总反应为:2H2+O2===2H2O,负极反应:H2+CO32--2e-===H2O+CO2。下列说法正确的是
| A.电路中的电子经正极、熔融的K2CO3、负极后再到正极,形成闭合回路 |
| B.电池放电时,电池中CO32-的物质的量将逐渐减少 |
| C.正极反应为2H2O+O2+4e-===4OH- |
| D.放电时CO32-向负极移动 |
下列反应的产物中,一定不存在同分异构体的是 
下列各组反应,属于同一反应类型的是
| A.由溴丙烷水解制丙醇,由丙烯和水反应制丙醇 |
| B.由甲苯硝化制对硝基甲苯,由甲苯遇高锰酸钾制苯甲酸 |
| C.由氯代环己烷制环己烯,由丙烯制1,2-二溴丙烷 |
| D.由乙酸和乙醇制乙酸乙酯,由苯甲酸乙酯水解制苯甲酸和乙醇 |
下列高聚物必须是由两种单体加聚而成的是 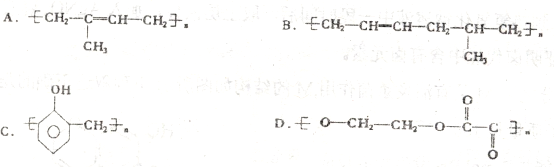
下列离子方程式正确的是
A.乙酸与碳酸氢钠溶液反应:H4+HCO3- CO2↑+H2O CO2↑+H2O |
| B.醋酸溶液与新制氢氧化铜反应:CH3COOH+OH-→CH3COO-+H2O |
| C.苯酚溶液与Na2CO3溶液:2C6H5OH+CO32-→2C6H5O-+CO2↑+H2O |
| D.甲醛溶液与足量的银氨溶液共热 |
HCHO+4[Ag(NH3)2]+4OH- CO32-+2NH4++4Ag↓+6NH3+2H2O
CO32-+2NH4++4Ag↓+6NH3+2H2O
针对下图所示乙醇分子结构,下述关于乙醇在各种化学反应中化学键断裂情况的说法不正确的是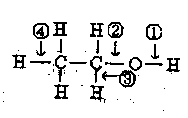
| A.与金属钠反应时,①键断裂 |
| B.与浓硫酸共热至170℃时,②、④键断裂 |
| C.与醋酸、浓硫酸共热时,②键断裂 |
| D.在Ag催化下与O2反应时,①、③键断裂 |