向ZnSO4溶液中加入Na2S溶液时,得到白色沉淀,然后向白色沉淀中滴加CuSO4溶液,发现沉淀变为黑色,则下列说法不正确的是
| A.白色沉淀为ZnS,黑色沉淀为CuS |
| B.利用该原理可实现一种沉淀转化为更难溶的沉淀 |
| C.上述现象说明ZnS的Ksp小于CuS的Ksp |
| D.该过程破坏了ZnS的溶解平衡 |
常温下已知两种一元弱酸HX和HY,如果向NaX溶液中通CO2气体 ,只能生成HX和NaHCO3;往NaY溶液中通入CO2则生成HY和Na2CO3。有关叙述正确的是
,只能生成HX和NaHCO3;往NaY溶液中通入CO2则生成HY和Na2CO3。有关叙述正确的是
| A.结合H+的能力:Y―>CO32―>X―>HCO3― |
| B.酸性由强至弱:HX>HY>H2CO3 |
C.溶液物质的量浓度 相同时碱性:NaX>Na2CO3>NaY>NaHCO3 相同时碱性:NaX>Na2CO3>NaY>NaHCO3 |
| D.NaX溶液中通入足量CO2后的离子浓度:c(X―)>c(Na+)>c(HCO3―)>c(OH―) |
在给定的四种溶液中,加入以下各种离子,各离子一定能在原溶液中大量共存的有
| A.滴加石蕊试液显红色的溶液:Fe3+、NH4+、Cl-、I- |
| B.pH值为1的溶液:Cu2+、Na+、Mg2+、NO3- |
| C.水电离出来的c(H+)=10-13mol/L的溶液:K+、HCO3-、Br-、Ba2+ |
| D.c(H+)2=Kw的溶液:K+、Al3+、Cl—、HCO3— |
25℃时,0.1mol/L稀醋酸加水稀释,右图坐标中的纵坐标y可以是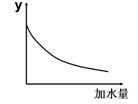
| A.溶液的pH |
| B.醋酸的电离平衡常数 |
| C.溶液的导电能力 |
| D.醋酸的电离程度 |
25℃时在五份蒸馏水 中分别加入适量的下列物质,所得实验结果如下表所示:
中分别加入适量的下列物质,所得实验结果如下表所示:
| 加入物质 |
HCl(aq) |
FeCl3 |
NaOH |
HCOONa |
C2H5OH |
| 溶液的pH |
3 |
4 |
10 |
11 |
未测定 |
| 水的电离程度 |
α1 |
α2 |
α3 |
α4 |
α5 |
加入物质后水的电离程度由大到小排列顺序正确的是
A.α3>α1>α5>α4>α2 B.α4>α2>α5>α3>α1
C.α2>α4>α5>α1>α3 D.α1>α3>α5>α2>α4
下列溶液蒸干后,能得到溶质固体的是
| A.AlCl3 | B.KHCO3 | C.Fe2(SO4)3 | D.NaClO |