下列表达式书写正确的是
| A.CaCO3的电离方程式:CaCO3=Ca2++CO32- |
B.HCO3-的电离方程式:HCO3-+H2O H3O++CO32- H3O++CO32- |
C.CO32-的水解方程式:CO32-+2H2O H2CO3+2OH- H2CO3+2OH- |
| D.CaCO3的沉淀溶解平衡表达式:CaCO3(s)=Ca2+(aq)+CO32-(aq) |
下列叙述正确的是
| A.同种元素的原子均具有相同的质子数和中子数 |
| B.不同元素的原子构成的分子只含极性键 |
| C.第三周期中的非金属元素的气态氢化物还原性越强,对应元素的最高价含氧酸酸性越弱 |
| D.第ⅠA族和第ⅦA族元素从上到下随原子序数递增,单质的沸点均逐渐升高 |
化学在生产和日常生活中有着重要的作用。下列有关的说法中不正确的是
| A.“嫦娥二号”中使用的碳纤维,是一种新型无机非金属材料 |
| B.氢氧化铁溶胶、含塑化剂的白酒、含有细菌的矿泉水均具有丁达尔效应 |
| C.“地沟油”经过加工处理后,可以用来制肥皂和生物柴油 |
| D.只要符合限量,“食用色素”、“碘元素”、“亚硝酸盐”可以作为某些食品的添加剂 |
下列说法正确的是( )
A.如图可表示水分解过程中的能量变化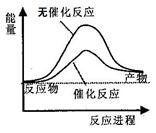 |
| B.若2C(s)+O2(g)=2CO(g)△H="-221.0" kJ/mol,则碳的燃烧热为110.5 kJ/mol |
| C.需要加热的反应一定是吸热反应,常温下能发生的反应一定是放热反应 |
| D.已知:Ⅰ:对于反应:H2(g)+Cl2(s)="2HCl" (g)△H="-" a kJ/mol, |
Ⅱ:
且a、b、c均大于零,则断开1molH-Cl键所需的能量为- a-b-c
从矿物学资料查得,一定条件下自然界存在如下反应:14CuSO4+5FeS2+12H2O=7X+5FeSO4+12H2SO4,下列说法正确的是( )
| A.X的化学式为CuS,它既是氧化产物又是还原产物 |
| B.5molFeS2发生反应,有10mol电子转移 |
| C.产物中的SO42-离子有一部分是氧化产物 |
| D.FeS2只作还原剂 |
下列离子方程式正确的是( )
A.小苏打溶液中加入少量石灰水:HCO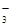 +Ca2++OH-=CaCO3↓+H2O +Ca2++OH-=CaCO3↓+H2O |
B.稀硝酸中加入过量铁粉: Fe+4H++NO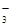 =Fe3++NO↑+2H2O =Fe3++NO↑+2H2O |
| C.溴化亚铁溶液中通入足量氯气:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- |
D.苯酚钠溶液中通入少量二氧化碳: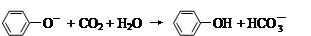 |