有Mg、Al、Fe、Cu四种金属,若两两混合,取混合物26g与足量稀硫酸反应,产生标准状况下H2 11.2L。此混合物的可能组成方式最多有
| A.2种 |
B.3种 |
C.4种 |
D.5种 |
对下列化学反应的热现象的说法正确的是
| A.所有的放热反应不加热都能进行 |
| B.任何化学反应的发生一定伴有能量变化 |
| C.吸热反应和放热反应都需要加热才能发生 |
| D.化学反应吸收或放出热量的多少与参加反应的物质的多少无关 |
下列反应不能设计成原电池的是
| A.2CH3OH+3O2 →2CO2+4H2O | B.NaOH+HCl = NaCl+H2O |
| C.Zn+2HCl = ZnCl2+H2↑ | D.4Al+3O2+6H2O = 4Al(OH)3 |
下列变化过程和对应的能量转化关系错误的是
| A.植物光合作用:光能→生物质能 | B.太阳能热水器:太阳能→电能 |
| C.石灰石高温分解:热能→化学能 | D.铅蓄电池:化学能→电能 |
某元素二价阴离子的核外有18个电子,质量数为34,该元素的原子核中的中子数为
| A.16 | B.18 | C.20 | D.22 |
下列说法正确的是
| A.原子核外电子排布决定了该原子的化学性质 |
| B.根据原子序数可以推知该原子的中子数和其在周期表中的位置 |
C.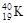 、 、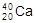 是具有相同质量数的同位素原子 是具有相同质量数的同位素原子 |
| D.所有的原子核都是由质子和中子组成的 |