化学和环境保护、食品营养、材料应用等密切相关。
(1)防治环境污染、改善生态环境已成为全人类的共识。
①下列各项中,完成空气质量报告时不需要监测的是 (填字母)。
A.可吸入颗粒物的浓度
B.二氧化氮的浓度
C.二氧化碳的浓度
②下列做法中不利于改善环境质量的是 (填字母)。
A.将废旧电池进行深埋处理
B.充分利用太阳能等清洁能源
C.给汽车加装尾气催化净化装置
③工业废水需处理达标后才能排放。轧钢厂排出的废水主要是含盐酸的酸性废水,处理此废水可采用的方法是 (填字母)。
A.沉淀法 B.中和法 C.氧化还原法
(2)营养平衡、合理用药是保证人体健康和生活质量的重要途径。
①人体需要的营养素主要有糖类、 、蛋白质、无机盐、维生素和水。在氢、钠、铁这三种元素中,属于人体生命活动必需微量元素的是 。
②下列物质中,具有解热镇痛疗效的是 (填字母)。
A.氨基酸 B.阿斯匹林 C.青霉素
③有些药片常用淀粉作为黏合剂,淀粉进入人体后在人体内酶的催化作用下逐步水解,最终转化为 (填物质的名称)。维生素C能防治坏血病并具有还原性,验证维生素C有还原性可以使用淀粉溶液和 试剂共同完成。
(3))材料是人类社会发展的物质基础,材料科学的发展离不开化学。
①陶瓷、水泥和普通玻璃都是生活中最常见的材料,它们属于 (填字母)。
A.金属材料 B.无机非金属材料 C.有机高分子材料
制造普通玻璃时,需要的主要原料有纯碱、石灰石和 (填化学式)。
②钢铁制品在潮湿的空气中发生 (填“化学”或“电化学”)腐蚀是造成钢铁腐蚀的主要原因。硬铝(一种铝合金)是制造飞机和宇宙飞船的理想材料,和纯铝相比,硬铝的强度 (填“低”、“高”或“无法确定”),具有较强的抗腐蚀能力。
③在尼龙、棉花、涤纶这三种物质中,属于天然纤维的是 。橡胶是制造轮胎的重要原料,天然橡胶通过 (填“硫化”、“氧化”或“老化”)措施可增大其强度、弹性和化学稳定性等。“白色污染”已成为当今社会的一大公害,“白色污染”主要是 (填“废塑料制品”、“废橡胶制品”或“生活垃圾”)造成的。
【化学选修-化学与技术】(15分)铈、铬、钛、镍虽不是中学阶段常见的金属元素,但在工业生产中有着重要作用。
(1)二氧化铈 (CeO2)在平板电视显示屏中有着重要应用。CeO2在稀硫酸和H2O2的作用下可生成Ce3+,CeO2在该反应中作______________剂。
(2)自然界中Cr主要以+3价和+6价存在。+6价的Cr能引起细胞的突变,可以用亚硫酸钠将其还原为+3价的铬。写出过程中的离子方程式:。
(3)钛(Ti)被誉为“二十一世纪的金属”,工业上在550℃时用钠与四氯化钛反应可制得钛,该反应的化学方程式是。
(4)NiSO4·xH2O是一种绿色易溶于水的晶体,广泛用于镀镍、电池等,可由电镀废渣(除镍外,还含有铜、锌、铁等元素)为原料获得。操作步骤如下: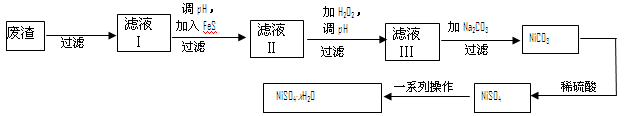
①向滤液Ⅰ中加入FeS是为了除去Cu2+、Zn2+等杂质,除去Cu2+的离子方程式为。
②对滤液Ⅱ先加H2O2再调pH,加H2O2的目的是,调pH的目的是。
③滤液Ⅲ溶质的主要成分是NiSO4,加Na2CO3过滤后,再加适量稀硫酸溶解又生成NiSO4,这两步操作的目的是。
以下是处于研究阶段的“人工固氮”的新方法.N2在催化剂表面与水发生反应:
2N2(g)+6H2O(l)⇌4NH3(g)+3O2(g) △H="+" 1530.4kJ/mol;完成下列填空:
(1)该反应平衡常数K的表达式.
(2)上述反应达到平衡后,保持其他条件不变,升高温度,重新达到平衡,则.
a.平衡常数K增大
b.H2O的浓度减小
c.容器内的压强增大
d.v逆(O2)减小
(3)研究小组分别在四个容积为2升的密闭容器中,充入N2 1mol、H2O 3mol,在催化剂条件下进行反应3小时.实验数据见下表:
| 序号 |
第一组 |
第二组 |
第三组 |
第四组 |
| t/℃ |
30 |
40 |
50 |
80 |
| NH3生成量/(10﹣6mol) |
4.8 |
5.9 |
6.0 |
2.0 |
第四组实验中以NH3表示反应的速率是,与前三组相比,NH3生成量最小的原因可能是.
(4)氨水是实验室常用的弱碱.
①往CaCl2溶液中通入CO2至饱和,无明显现象.再通入一定量的NH3后产生白色沉淀,此时溶液中一定有的溶质是.请用电离平衡理论解释上述实验现象.
②向盐酸中滴加氨水至过量,该过程中离子浓度大小关系可能正确的是.
a.c(C1﹣)=c(NH4+)>c(H+)=c(OH﹣)
b.c(C1﹣)>c(NH4+)=c(OH﹣)>c(H+)
c.c(NH4+)>c(OH﹣)>c(C1﹣)>c(H+)
d.c(OH﹣)>c(NH4+)>c(H+)>c(C1﹣)
X、Y、Z、W是短周期的四种元素,有关他们的信息如下表所示.
| 元素 |
部分结构知识 |
部分性质 |
| X |
X的单质由双原子分子构成,分子中有14个电子 |
X有多种氧化物,如XO、XO2、X2O4等;通常情况下XO2与X2O4共存 |
| Y |
Y原子的次外层电子数等于最外层电子数的一半 |
Y能形成多种气态氢化物 |
| Z |
Z原子的最外层电子数多于4 |
Z元素的最高正化合价与最低负化合价代数和等于6 |
| W |
W原子的最外层电子数等于2n﹣3(n为原子核外电子层数) |
化学反应中W原子易失去最外层电子形成Wn+ |
填写下列空白:(提示:不能用字母X、Y、Z、W作答)
(1)X的气态氢化物分子的电子式是,Z元素在周期表中的位置是。
(2)X、Y、Z三元素的最高价氧化物的水化物酸性由强到弱的顺序是。
(3)常温时,W的硫酸盐溶液的pH7(填“=”、“>”或“<”),理由是:(用离子方程式表示)。
(4)实验室用X的氢化物的水溶液制取W的氢氧化物的方法是(用离子方程式表示).
(5)25℃、101kPa时,32g Y的最低价气态氢化物完全燃烧生成稳定的氧化物时放出1780.6kJ的热量,写出该反应的热化学方程式。
(12分)近年来我国汽车拥有量呈较快增长趋势,NOx是汽车尾气中的主要污染物之一。
(1)汽车发动机工作时会引发N2和O2反应,其能量变化示意图如下:
①写出该反应的热化学方程式,该反应的△S0(填“>”、“<”或“=”);
②根据下图所示,只改变条件R,当N2的转化率从a3到a1时,平衡常数K。
| A.可能增大 |
| B.一定不变 |
| C.可能不变 |
| D.可能减小 |
E.增大、减小、不变均有可能
(2)氮气是合成氨的原料之一,合成氨反应:N2(g)+3H2 (g) 2NH3(g) △H<0,500℃时将1molN2与1molH2充入容积为1L的密闭容器中发生反应,达到平衡后NH3的体积分数为20%。若升高温度至800℃,达到新的平衡时,H2的转化率(填“增大”、“减小”或不变,下同),N2的体积分数。
2NH3(g) △H<0,500℃时将1molN2与1molH2充入容积为1L的密闭容器中发生反应,达到平衡后NH3的体积分数为20%。若升高温度至800℃,达到新的平衡时,H2的转化率(填“增大”、“减小”或不变,下同),N2的体积分数。
(3)在汽车上安装高效催化转化器,将有毒气体转化为无毒气体,可有效降低NOx的排放。某研究性学习小组用气体传感器测得不同时间NO和CO的浓度如下表:
| 时间/s |
0 |
1 |
2 |
3 |
4 |
5 |
| c(NO)(×10-4mol·L-1) |
10.0 |
4.50 |
2.50 |
1.50 |
1.00 |
1.00 |
| c(CO)(×10-3 mol·L-1) |
3.60 |
3.05 |
2.85 |
2.75 |
2.70 |
2.70 |
请回答下列问题:
①写出反应的化学方程式。
②前2 s内的平均反应速率ν(N2) =。
无机化合物A和金属B是中学化学常见的固体,其中A显淡黄色。相同质量的A、B都能与液体C反应放出气体,两气体又能恰好完全反应生成C。利用B在高温下的挥发性,可通过它的碳酸盐和焦炭在真空环境中来制备B。化合物D可作为有机反应中的脱氢试剂,1molD和1mol NH4Cl反应生成2mol气体E和1molB的氯化物。已知标准状况下气体E的密度为0.76g·L-1。
请回答下列问题:
(1)题中制备B的化学方程式为。
下列物质能替代焦炭的是。
A.NaB.H2C.KMnO4D.Cl2
(2)写出D与过量盐酸反应的化学方程式。
(3)B与E在一定条件下(填“可能”或“不可能”)直接发生反应产生D,判断理由是。