下列实验现象与氧化还原反应有关的是
| A.SO2通入品红溶液中,溶液褪色 |
| B.新制氯水密闭放置一段时间后浅黄绿色消失 |
| C.向Fe2(SO4)3溶液中滴加NaOH溶液,生成红褐色沉淀 |
| D.向硅酸钠溶液中滴加适量的稀盐酸,有透明的凝胶形成 |
中药狼把草全草浸剂给动物注射,有镇静、降压及轻度增大心跳振幅的作用。有机物M是中药狼把草的成分之一,其结构如图所示。下列叙述不正确的是
| A.M是芳香族化合物,它的分子式为C9H5O4Cl |
| B.1molM最多能与含2molBr2的溴水发生反应 |
| C.1molM分别与足量的NaOH溶液、Na2CO3溶液反应,消耗两种物质的物质的量分别为4mol、2mol |
| D.在一定条件下能发生取代、加成、水解、氧化等反应Cl |
某单烯烃和氢气完全加成后得到的饱和烃是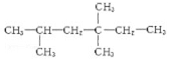 ,该烯烃可能有的结构有
,该烯烃可能有的结构有
| A.2种 | B.3种 | C.4种 | D.5种 |
将有机物的混合物在一定条件下反应:①甲醇与乙醇的混合物与浓硫酸加热得醚;②乙烷与氯气光照下取代;③氨基乙酸和丙氨酸生成二肽;④苯和液溴、Fe粉反应。所生成的有机物的种类由多到少的顺序是
| A.③②④① | B.③②①④ | C.②③①④ | D.①②③④ |
下图表示4-溴环己烯所发生的4个不同反应,其中产物只含有一种官能团的反应是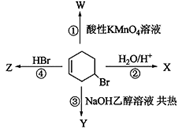
| A.①② | B.②③ | C.③④ | D.①④ |
某中性有机物C8H16O2在稀硫酸作用下加热得到M和N两种物质,N经氧化最终可得到M,则该中性有机物的结构可能有
| A.1种 | B.2种 | C.3种 | D.4种 |