A、B、X、Y均为中学阶段的常见物质,它们之间的转化关系如下图所示:
请回答下列问题:
(1)若A为金属单质,B为非金属氧化物,则该反应的化学方程式为 ;请写出质量数为26的A的一种核素符号 。
(2)若A为金属单质,B为黑色磁性晶体,则该反应的化学方程式为 ;请写出A与氢氧化钠溶液反应的离子方程式 ;
(1)将1.8g碳置于2.24L(标准状况)O2中充分燃烧,至全部反应物耗尽,测得放出热量30.65kJ,已知:C(s)+O2(g) CO2(g)△H=-393.0 kJ·mol—1,请写出CO完全燃烧的热化学方程式 。
CO2(g)△H=-393.0 kJ·mol—1,请写出CO完全燃烧的热化学方程式 。
(2)光气 (COCl2)是一种重要的化工原料,用于农药、医药、聚酯类材料的生产,工业上通过Cl2(g)+CO(g) COCl2(g) △H<0制备。右图为某次模拟实验研究过程中容积为1L的密闭容器内各物质的浓度随时间变化的曲线。回答下列问题:
COCl2(g) △H<0制备。右图为某次模拟实验研究过程中容积为1L的密闭容器内各物质的浓度随时间变化的曲线。回答下列问题: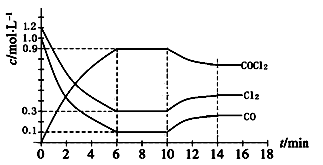
①若保持温度不变,在第8min 加入体系中的三种物质各1mol,则平衡 移动(填“向正反应方向”、“向逆反应方向”或“不”);
②若将初始投料浓度变为c(Cl2)=0.8mol/L、c(CO)=0.6 mol/L、c(COCl2)= mol/L,保持反应温度不变,则最终达到化学平衡时,Cl2的体积分数与上述第6 min时Cl2的体积分数相同;
③比较第8 min反应温度T(8)与第15 min反应温度T(15)的高低:T(8) T(15)(填“<”、“>”或“=”)。
(3)将燃煤废气中的CO2转化为二甲醚的反应原理为:
2CO2(g) + 6H2(g)  CH3OCH3(g) + 3H2O(g)。
CH3OCH3(g) + 3H2O(g)。
①已知一定条件下,该反应中CO2的平衡转化率随温度、投料比[n(H2) / n(CO2)]的变化曲线如图:在其他条件不变时,请在右图中画出平衡时CH3OCH3的体积分数随投料比[n(H2) / n(CO2)]变化的曲线图。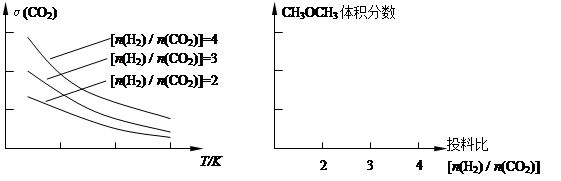
②二甲醚(CH3OCH3)燃料电池可以提升能量利用率,二甲醚酸性介质燃料电池的负极反应式为 。
(4)常温下,将a mol/L的醋酸与b mol/L Ba(OH)2溶液等体积混合,充分反应后,溶液中存在2c(Ba2+)=c(CH3COO-),则该混合溶液中醋酸的电离常数Ka= (用含和的代数式表示)。
一种含铝、锂、钴的新型电子材料,生产中产生的废料数量可观,废料中的铝以金属铝箔的形式存在;钴以Co2O3·CoO的形式存在,吸附在铝箔的单面或双面;锂混杂于其中。从废料中回收氧化钴(CoO)的工艺流程如图所示:
(1)过程I中采用NaOH溶液溶出废料中的Al,反应的离子方程式为 。
(2)过程Ⅱ中加入稀H2SO4酸化后,再加入Na2S2O3溶液浸出钴。则浸出钴的化学反应方程式为(产物中只有一种酸根) 。在实验室模拟工业生产时,也可用盐酸浸出钴,但实际工业生产中不用盐酸,请从反应原理分析不用盐酸浸出钴的主要原因 。
(3)过程Ⅲ得到锂铝渣的主要成分是LiF和Al(OH)3,碳酸钠溶液在产生Al(OH)3时起重要作用,请写出该反应的离子方程式 。
(4)碳酸钠溶液在过程Ⅲ和Ⅳ中所起作用有所不同,请写出在过程IV中起的作用是_____________。
(5)在Na2CO3溶液中存在多种粒子,下列各粒子浓度关系正确的是____________(填序号)。
| A.c(Na+) = 2c(CO32-) | B.c(Na+) > c(CO32-) > c(HCO3-) |
| C.c(OH-) > c(HCO3-) > c(H+) | D.c(OH-)-c(H+) = c(HCO3-) + 2c(H2CO3) |
(6)CoO溶于盐酸可得粉红色的CoCl2溶液。CoCl2含结晶水数目不同而呈现不同颜色,利用蓝色的无水CoCl2吸水变色这一性质可制成变色水泥和显隐墨水。下图是粉红色的CoCl2·6H2O晶体受热分解时,剩余固体质量随温度变化的曲线,A物质的化学式是____________。
【化学—选修5有机化学基础】
物质A(C5H8)是形成天然橡胶的单体,它的一系列反应如下图所示(部分反应条件略去):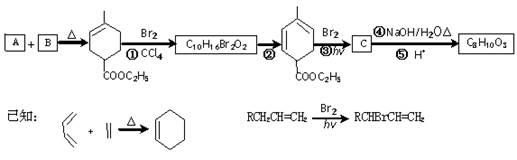
请按要求回答下列问题:
(1)反应①和③的反应类型分别是_____________、_____________。
(2)B的分子式为_________________;B形成高聚物的结构简式为_______________________。
(3)反应②的化学方程式为________________________。
(4)C为一溴代物,分子中含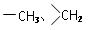 均2个,反应④的化学方程式为_____________________。
均2个,反应④的化学方程式为_____________________。
(5)A的名称是______________________。
写出所有符合下列条件的A的同分异构体的结构简式:____________________
①环状②核磁共振氢谱显示有2种氢原子③不含立体异构________________________。
【化学——选修3:物质结构与性质】
卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们。
(1)卤族元素位于元素周期表的________区;溴的价电子排布式为________________。
(2)在一定浓度的溶液中,氢氟酸是以二分子缔合(HF)2形式存在的。使氢氟酸分子缔合的作用力是____________。
(3)请根据下表提供的第一电离能数据判断,最有可能生成较稳定的单核阳离子的卤素原子是_________(写出名称)。
| 氟 |
氯 |
溴 |
碘 |
|
| 第一电离能(kJ/mol) |
1681 |
1251 |
1140 |
1008 |
(4)已知碘酸(HIO3)和高碘酸(H5IO6)的结构分别如图I、II所示: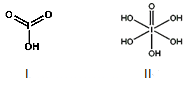
请比较二者酸性强弱:HIO3_____ H5IO6(填“>”、 “<”或“=”)。
(5)硼酸(H3BO3)是一种片层状结构的白色晶体,层内的H3B03分子间通过氢键相连(如下图)。则1 molH3BO3的晶体中有 mol氢键。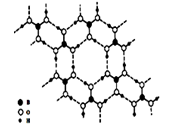
硼酸溶于水生成弱电解质一水合硼酸B(OH)3·H2 O,它电离生成少量[B(OH)4]一和H+,则 [B(OH)4]一含有的化学键类型为 。
(6)如图所示的二维平面晶体示意图中表示化学式为AX3的是________。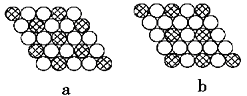
【化学——选修2:化学与技术】
由黄铜矿(主要成分是CuFeS2)炼制精铜的工艺流程示意图如下:
(1)在反射炉中,把铜精矿砂和石英砂混合加热到10000C左右,黄铜矿与空气反应生成Cu和Fe的低价硫化物,且部分Fe的硫化物转变为低价氧化物,该过程中两个主要反应的化学方程式分别是 , 反射炉内生成炉渣的主要成分是 ;
(2)冰铜(Cu2S和FeS互相熔合而成)含Cu量为20%~50%。转炉中,将冰铜加熔剂(石英砂)在1200°C左右吹入空气进行吹炼。冰铜中的Cu2S被氧化成Cu2O,生成的Cu2O与Cu2S反应,生成含Cu量约为98.5%的粗铜,该过程发生反应的化学方程式分别是 ; ;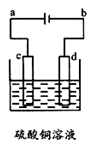
(3)粗铜的电解精炼如图所示。在粗铜的电解过程中,粗铜板应是图中电极 (填图中的字母);在电极d上发生的电极反应式为 ;若粗铜中还含有Au、Ag、Fe,它们在电解槽中的存在形式和位置为 。