下列实验操作中正确的是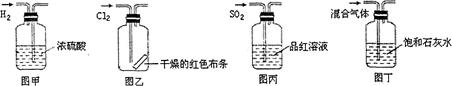
| A.图甲所示,可得到干燥的氢气 |
| B.图乙所示,可以验证氯气的漂白性 |
| C.图丙所示,可以验证SO2的漂白性 |
| D.图丁所示,若石灰水变浑浊,证明混合气体中一定含有CO2 |
2g氢气完全燃烧生成液态水时可放出285.8KJ的热量,下列热化学方程式正确的是
| A.2H2(g)+O2(g)==2H2O(g)△H=-571.6kJ/mol |
| B.2H2(g)+O2(g)==2H2O(l)△H=-285.8kJ/mol |
| C.H2+1/2 O2==H2O△H=-285.8kJ/mol |
| D.2H2(g)+O2(g)==2H2O(l)△H=-571.6kJ/mol |
下列说法中错误的是
| A.化学反应中的能量变化通常表现为热量的变化 |
| B.化学键的断裂和形成是化学反应中能量变化的主要原因 |
| C.需要加热才能发生的反应一定是吸热反应 |
| D.反应物总能量和生成物总能量相对大小决定该反应是吸热反应还是放热反应 |
某元素的原子序数为7,对它的认识不正确的是
| A.它处于元素周期表中第二周期VA族 |
| B.它的最高正价为+5,负价为-3 |
| C.它的最高价氧化物对应水化物是一种强酸 |
| D.它的非金属性比磷弱比氧强 |
下列叙述错误的是
| A.NaOH、Mg (OH)2、Al (OH)3碱性依次减弱 |
| B.Na、Mg、Al原子半径依次减小 |
| C.H3PO4、H2SO4、HClO4酸性依次增强 |
| D.HCl、HBr、HI稳定性依次增强 |
表示下列微粒结构的图式,不正确的是
| A.二氧化碳的结构式:O=C=O | B.钠离子的结构示意图: |
C.H2O分子的比例模型: |
D.氯化氢分子的电子式: |