盖斯定律在生产和科学研究中有很重要的意义,有些反应的反应热虽然无法直接测得,但可以用盖斯定律间接求得。已知3.6 g碳在6.4 g的氧气中燃烧,至反应物耗尽,并放出x kJ热量;已知每摩尔单质碳完全燃烧生成CO2放出热量为y kJ,则1 mol C与O2反应生成CO的反应热ΔH为
| A.-y kJ·mol-1 | B.-(10x-y)kJ·mol-1 |
| C.-(5x-0.5y)kJ·mol-1 | D.+(10x-y)kJ·mol-1 |
某试管中盛装的是红棕色气体(可能是两种气体的混合物),当倒扣在盛水的水槽中时,试管内水面上升,但不能充满试管,当试管内鼓入氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,则原来试管中盛装的气体是()
| A.一定是O2与NO2的混合气体 | B.可能是NO和NO2的 混合气体 混合气体 |
| C.可能是N2与NO2的混合气体 | D.只可能是NO2一种气体 |
下表各组物质中,物质之间不可能实现如图所示转化的是( )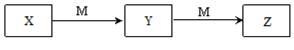
| 选项 |
X |
Y |
Z |
M |
| ① |
Al3+ |
Al(OH)3 |
[Al(OH)4]- |
NaOH |
| ② |
[Al(OH)4]- |
Al(OH)3 |
Al3+ |
HCl |
| ③ |
Fe |
FeCl2 |
FeCl3 |
Cl2 |
| ④ |
Cl2 |
FeCl3 |
FeCl2 |
Fe |
| ⑤ |
NaOH |
Na2CO3 |
NaHCO3 |
CO2 |
| ⑥ |
NH3 |
NO |
NO2 |
O2 |
| ⑦ |
C2H5OH |
CH3CHO |
CH3COOH |
O2 |
| ⑧ |
H2S |
SO2 |
SO3 |
O2 |
A.只有③ B. ③④ C. ④⑥⑧ D. ②③⑦
下列叙述正确的是()
①装置甲可防止铁钉生锈 ②装置乙可除去乙烯中混有的乙炔
③装置丙可验证HCl气体在水中的溶解性 ④装置丁可用于实验室制取乙酸乙酯
⑤装置戊可用于收集H2、CO2、Cl2、HCl、NO2等气体
| A.①③⑤ | B.③⑤ | C.①②④ | D.③④ |
实验室一瓶固体M的标签右半部分已被腐蚀,剩余部分只看到“Na2S”字样(如图所示)。已知,固体M只可能是Na2SO3、Na2SiO3、Na2SO4中的一种。若取少量固体M配成稀溶液进行有关实验,下列说法不正确的是( )
| A.只用盐酸一种试剂就可以确定该固体M的具体成分 |
| B.往溶液中通入二氧化碳,若有白色沉淀,则固体M为Na2SiO3 |
| C.往溶液中加入稀硝酸酸化的BaCl2,若有白色沉淀,则固体M为Na2SO4 |
| D.用pH试纸检验,若pH=7,则固体M一定是Na2SO4 |
已知反应:①101kPa时,2C(s)+O2(g)=2CO(g);△H=-221 kJ/mol
②稀溶液中,H+(aq)+OH-(aq)=H2O(1);△H=-57.3 kJ/mol
③红磷的化学式为P,白磷的化学式为P4,已知
P4(s)+5O2(g)="P4O10(s)" △H=-3093.2 kJ/mol
4P (s)+5O2(g)="P4O10(s)" △H=-2954.0 kJ/mol
下列结论正确的是()
| A.由于红磷转化为白磷是放热反应,等质量的红磷能量比白磷低 |
| B.稀硫酸与稀NaOH溶液反应的中和热△H=57.3 kJ/mol |
| C.碳的燃烧热大于-110.5 kJ/mol |
| D.稀醋酸与稀NaOH溶液反应生成1 mol水,△H 大于 -57.3 kJ/mol |