A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去)。
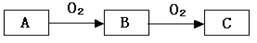
(1)若A是一种黄色单质固体,则B→C的化学方程式为 。
(2)若A是一种活泼金属,C是淡黄色固体,则C的名称为 ,试用化学方程式表示该物质与二氧化碳气体的反应 。将C长期露置于空气中,最后将变成物质D,D的化学式为 。现有D和NaHCO3的固体混合物10g,加热至质量不再改变,剩余固体质量为9.38 g,D的质量分数为 。
(3)若C是红棕色气体,A可能是一种能使湿润的红色石蕊试纸变蓝的气体。下图是实验室制取A气体的装置,请结合所学知识,回答下列问题:

①收集A的方法是 ,验证A是否已经收集满的方法是 (任写一种)。
②写出实验室制取A的化学方程式 。
③若有5.35g氯化铵参加反应,则产生的A气体在标准状况下的体积为 L。
④试写出C与水反应的化学方程式 ,反应可得到酸X,X是 电解质(填“强”或“弱”)。如下图:足量X的浓溶液与Cu反应,写出烧瓶中发生反应的离子方程式 。实验完毕后,试管中收集到的气体的主要成分为 (写化学式)。

(8分)(1)A、B两元素均位于周期表中第三周期,它们的原子核外最外层电子数之和为7,其中A元素的原子核外最外层电子数为1个,两者间可形成化合物A2B。根据以上条件回答:
①写出A、B的元素符号:A,B
②写出化合物A2B的电子式。
(2) 现有A、B、C、D四种物质,它们之间能发生如下图所示的转化关系
溶液B、C中都含有金属元素E,溶液B的颜色为黄色。请根据以上信息回答下列问题:
①写出金属E元素符号:
②写出金属A和溶液B反应的离子方程式:
③为了检验溶液B中金属阳离子,通常加入的试剂是
(4分)(1) 写出乙醇与乙酸反应生成酯的化学方程式。
(2) 写浓盐酸与二氧化锰加热反应来制取氯气的化学方程式_________。
如右图,一定温度下,分别往容积均为 5L 的甲(恒压容器)、乙(恒容容器)中加入 0.5mol无色的N2O4气体,立即出现红棕色。当反应进行到 2s时,测得乙容器中N2O4的浓度为 0.09mol·L-1。经过 60s,乙容器中的反应达到平衡。(反应过程中两个容器的温度均保持恒定)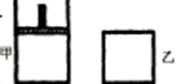
(1)容器中气体出现红棕色的原因(用化学方程式表示)是:。(2)前 2s内乙容器中以N2O4的浓度变化表示的反应速率为。
(3)达到平衡时,甲容器中反应所需的时间60s(填“大于”、“小于”或“等于”,以下同);容器内N2O4的浓度甲乙;反应过程中吸收的能量甲乙。
已知单质铁和硫粉反应时需用酒精灯加热反应方能发生,但在铁粉和硫粉开始化合后把酒精灯撤去,反应仍可进行完全。则此反应为____反应。(填“吸热”“放热”)原因是________。
1g碳与适量水蒸气反应生成CO和H2,需吸收10.94KJ热量,此反应的热化学方程式为