下列说法错误的是
| A.浓硝酸在光照条件下变黄,说明浓硝酸不稳定,生成的有色产物能溶于浓硝酸 |
| B.在KI-淀粉溶液中通入氯气,溶液变蓝,是因为生成的单质碘与淀粉发生显色反应 |
| C.在某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成,说明溶液中一定含SO42- |
| D.实验室可用氯化铵与氢氧化钙加热制取氨气 |
以下六种饱和溶液①Ba(NO3)2 ②Ca(OH)2 ③Na2SiO3 ④NaAlO2 ⑤Na2CO3 ⑥ H3和NaCl,分别持续通入CO2,最终得到沉淀或析出晶体的是
| A.①③④⑥ | B.②③④⑥ | C.③④⑤⑥ | D.②③④⑤ |
在气体参与的反应中,能使反应物中活化分子数和活化分子百分数同时增大的方法是
①增大反应物的浓度 ②升高温度 ③增大压强 ④移去生成物 ⑤加入催化剂
| A.①②③ | B.①②③⑤ | C.①②③④⑤ | D.②⑤ |
Al、Fe、Cu都是重要的金属元素。下列说法正确的是
| A.制备AlCl3、FeCl3、CuCl2均不能采用将溶液直接蒸干的方法 |
| B.三者的单质放置在空气中均只生成氧化物 |
| C.工业上,三者的单质目前都使用热还原法制得 |
| D.电解AlCl3、FeCl3、CuCl2的混合溶液时阴极上依次析出Cu、Fe、Al |
NA代表阿伏加德罗常数,下列有关叙述错误的是
| A.1mol 固体NaHSO4含有的阴阳离子总数为2NA |
| B.标准状况下22.4L CH4和C2H4的混合气体所含氢原子数为4NA |
| C.常温常压下,3.4gNH3中含N—H键数目为0.6NA |
| D.56 g铁粉在1mol氯气中充分燃烧,失去的电子数为3NA |
下列有关化学用语的表示正确的是
A.N2的电子式: |
B.CH4的比例模型: |
| C.中子数为45的溴原子:45 35Br |
D.对羟基苯甲酸的结构简式: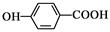 |