锶(Sr)是人体必需的微量元素,其单质和化合物的化学性质与钙、钡的相似。实验室用含碳酸锶的废渣(含SrCO3 38.40%,SrO12.62%,CaCO3 38.27%,BaCO3 2.54%,其它不溶于硝酸的杂质8.17%)制备硝酸锶粗品的部分实验过程如下:
(1)市售浓硝酸的质量分数为65%,密度为1.4g/cm3,要配制30%稀硝酸500mL,还需要查阅的数据是 ,若配制过程中不使用天平,则必须要计算的数据是 ,必须要使用的仪器是 。
已知两种盐的溶解度(g/100 g水)如下表
| 温度/℃物质 |
0 |
20 |
30 |
45 |
60 |
80 |
100 |
| Sr(NO3)2 |
28.2 |
40.7 |
47 |
47.2 |
48.3 |
49.2 |
50.7 |
| Ca(NO3)2·4H2O |
102 |
129 |
152 |
230 |
300 |
358 |
408 |
(2)由浸取后得到的混合物制备硝酸锶粗品的实验步骤依次为:过滤、 、 、洗涤,干燥。
已知,硝酸钙能溶于有机溶剂A中。式量:Sr(NO3)2–212、Ba(NO3)2–261、Ca(NO3)2–164
(3)制得的硝酸锶粗品中含少量Ca(NO3)2、Ba(NO3)2等杂质。测定硝酸锶纯度的实验如下:称取5.39g硝酸锶样品,加入足量的有机溶剂A,经过滤、洗涤、干燥后,剩余固体5.26g,将此固体配成250 mL的溶液,取出25.00 mL,调节pH为7,加入指示剂,用浓度为0.107mol/L的碳酸钠溶液滴定至终点,消耗碳酸钠溶液22.98mL。
滴定过程的反应:Sr2++CO32-→ SrCO3↓ Ba2++CO32-→ BaCO3↓
①滴定选用的指示剂为 ,滴定终点观察到的现象为 。
②该硝酸锶粗品中,硝酸锶的质量分数为 (小数点后保留两位)。若滴定前样品中Ca(NO3)2没有除尽,所测定的硝酸锶纯度将会 (填“偏高”、“偏低”或“不变”)。
(13 分)有一包固体粉末,由CaCO3、Na2SO4、KCl、Ba (NO3)2、CuSO4中的三种物质组成,取样品进行如下实验:
(1)写出实验过程中发生反应的化学方程式:。
(2)固体粉末中一定不存在的物质是;一定存在的物质是;
(3)将固体粉末可能的组合填入下表:(可以不填满,也可以再补充。)
| 序号 |
化学式 |
| Ⅰ |
|
| Ⅱ |
|
| Ⅲ |
(4)请设计一个实验进一步确定混合物的组成,简述实验步骤、现象和结论。
在一定温度下,将2molN2和6molH2充入固定容积的密闭容器中,发生 N2(g)+3H2(g)2NH3(g),达到化学平衡后,若保持温度不变,令a、b、c分别为N2、H2、NH3的物质的量,重新建立平衡,混合物中个物质的量仍和上述平衡相同,填空
N2(g)+3H2(g)2NH3(g),达到化学平衡后,若保持温度不变,令a、b、c分别为N2、H2、NH3的物质的量,重新建立平衡,混合物中个物质的量仍和上述平衡相同,填空
(1)若a=0,b=0,则c="———"
⑵、若a=1, c =2,则 b =————
⑶、若a、 b 、 c取值必须满足的一般条件为(用两个式子表示,一个只含a和c,一个只含b和c )————————、 ————————。
向2L密闭容器中通入amol 气体 A和bmol气体B,在一定条件下发生反应;
已知:平均反应速率 ;反应2min 时,A的浓度减少了
;反应2min 时,A的浓度减少了 ,B的物质的量减少了
,B的物质的量减少了 mol,有a mol D生成。回答下列问题
mol,有a mol D生成。回答下列问题
(1)反应2min内,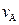 =,
=, ;
;
(2)化学方程式中,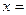 、
、 、
、 、
、 ;
;
(3)反应平衡时,D为2a mol,则B的转化率为;
(4)如果只升高反应温度,其他反应条件不变,平衡时D为 1.5a mol,则该反应的
0;(填“>”、“<”或“=”)
(5)如果其他条件不变,将容器的容积变为1L,进行同样的实验,则与上述反应比较:
①反应速率(填“增大”、“减小”或“不变”),理由是;
②平衡时反应物的转化率(填“增大”、“减小”或“不变”),理由是。
右图所表示在密闭容器中反应:2SO2(g)+O2(g)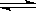 2SO3(g)ΔH<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a ~b过程中改变的条件可能是;b ~c过程中改变的条件可能是;若增大压强时,反应速度变化情况画在c~d处.
2SO3(g)ΔH<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a ~b过程中改变的条件可能是;b ~c过程中改变的条件可能是;若增大压强时,反应速度变化情况画在c~d处. 
18.在一定温度、一定体积的密闭容器中,对于N2(g)+3H2(g) 2NH3(g)的反应,达到平衡
2NH3(g)的反应,达到平衡
的标志是。
| A.生成氨的速率与NH3的分解速率相等 | B.断开一个N≡N键的同时有6个N—H键生成 |
| C.N2、H2、NH3百分含量不再变化 | D.总压强不变 |
E.N2、H2、NH3分子数之比为1∶3∶2的状态 F.N2、H2、NH3的浓度相等
G.N2、H2不再起反应 H.v(N2)= v(H2)
v(H2)
I.混合气体的密度不变 J.混合气体的平均摩尔质量不变