已知25℃时部分弱电解质的电离平衡常数数据如表所示:
| 化学式 |
CH3COOH |
H2CO3 |
HClO |
|
| 电离平衡常数 |
Ka=1.8×10-5 |
Kal=4.3×10-7 |
Ka2=5.6×10-11 |
Ka=3.0×10-8 |
回答下列问题:
(1)物质的量浓度均为0.1mol·L-1的四种溶液;a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
pH由小到大排列的顺序是_______________(用编号填写)。
(2)常温下,0.1mol·L-1CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是 。
A.c(H+ )
B.c(H+)/c(CH3COOH)
C.c(H+)·c(OH-)
D.c(OH-)/c(H+)
E.c(H+)·c(CH3COO-)/c(CH3COOH)
(3)体积均为100mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如下图所示,则同温度时HX的电离平衡常数_ ____(填“大于”、“小于”或“等于”)CH3COOH的电离平衡常数,理由是_____________________。
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)= mol·L-1(填精确值)。
(5)标准状况下,将1.12L CO2通入100mL 0.75mol·L-1的NaOH溶液中,则溶液中离子的浓度由大到小的顺序
某化学兴趣小组在探究常见物质转化时,发现部分物质存在如图所示的三角转化关系(部分反应物或生成物已略去):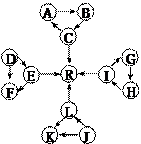
已知:①图中每个小三角形的三种物质中至少含有一种相同
元素,K与L含有完全相同的元素。②D、J为固体单质,
R为气体单质,其余物质为常见化合物。③A能使品红溶液
褪色,也能使澄清石灰水变浑浊。④E为淡黄色化合物,E
与C或L反应都能生成R。⑤I为氧化物,I与F或C都能
反应;G和L反应生成难溶物H,H具有较强的吸附性。根
据以上信息,回答下列问题:
(1)写出下列反应的化学方程式:
①C→A:
②L→R:。
(2)写出下列反应的离子方程式:①E→F:
②I→G:。
(3)常温下,测得一定浓度G溶液的pH=10,试用离子方程式表示其原因:。
A、B、C、D都是短周期元素,原子半径:D > C > A > B。已知:A、B同周期,A、C处于同一主族;C原子核内的质子数等于A、B原子核内的质子数之和;C原子最外层电子数是D原子最外层电子数的3倍。试回答:
(1)写出元素A的名称: A 。
(2)写出由B、D组成的两种化合物的电子式: 、 。
(3)C的固态氧化物属于 晶体。
(4)写出C的氧化物与D的氧化物对应的水化物反应的离子方程式:
。
(6分)已知C为贵重金属单质,下图中所有物质除C外含有的元素都是短周期元素,其中部分反应物或生成物省略,X是室内装潢材料中产生的主要有害气体之一,G是一种强碱。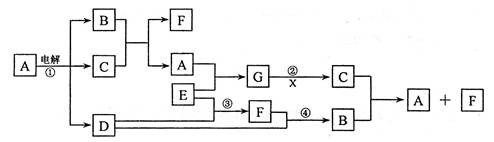
回答下列问题:
(1)写出下列物质的化学式:B、C、G;
(2)写出反应④的化学方程式。
(3)写出反应②的离子方程式:。
(4)用惰性电极电解A溶液,生成4.32gC的同时析出气体在标准状况下的体积是升。
已知: 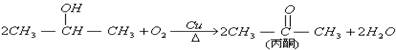
(丙酮不能发生银镜反应),现有如下转化关系: [F为高聚物,分子式为
[F为高聚物,分子式为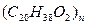 ]
]
请回答下列问题:
(1)反应类型:a,b。
(2)有机物A、D的结构简式:A,D。
(3)E→F的化学方程式。
“绿色奥运”是2008年北京奥运会的三大主题之一,其内涵是:要用保护环境、保护资源、保护生态平衡的可持续发展思想,指导运动会的工程建设、市场开发及大型活动等,尽可能减少对环境和生态系统的负面影响。
(1)下列措施符合“绿色奥运”这一主题的是:①多使用电动汽车;②工业和生活污水处理
后排放;③推广使用无铅汽油;④市区禁止机动车通行;⑤奥运村禁止使用高分子材料。
| A.①②③④⑤ | B.②④⑤ | C.①④⑤ | D.①②③ |
(2)2008年北京举行奥运会时,上海将使用1000辆以上清洁汽车和电动汽车,包括20-30辆燃料电池车。通常用的清洁燃料是指压缩天燃气和液化石油气,以渗透于多孔基质惰性导电物材料为电极,用35%~50%KOH为电解液,天然气和空气为原料,构成的电池为碱性燃料电池。请写出:
负极反应:;正极反应:;