制备水杨酸对正辛基苯基酯(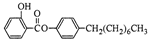 )如下:
)如下:
步骤一:将水杨酸晶体投入三颈烧瓶中,再加入氯苯,搅拌溶解后,加入无水三氯化铝。
步骤二:按图12所示装置装配好仪器,水浴加热控制温度在20~40℃之间,在搅拌下滴加SOCl2,反应制得水杨酰氯,该反应为: (水杨酸)+SOCl2→
(水杨酸)+SOCl2→ (水杨酰氯)+HCl↑+SO2↑
(水杨酰氯)+HCl↑+SO2↑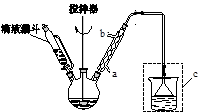
步骤三:将三颈烧瓶中的混合液升温至80℃,再加入对正辛苯酚[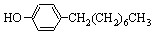 ],温度控制在100℃左右,不断搅拌。
],温度控制在100℃左右,不断搅拌。
步骤四:过滤、蒸馏、减压过滤;酒精洗涤、干燥。
(1)步骤一中加入三氯化铝的作用是 。
(2)实验时,冷凝管中的水应从 进 出(选填“a”或“b”);装置c的作用是 。
(3)步骤三中发生反应的化学方程式为 。
(4)步骤四减压过滤操作中,除烧杯、玻璃棒外,还必须使用的硅酸盐材料的仪器有 。
(5)步骤四减压过滤时,有时滤纸会穿孔,避免滤纸穿孔的措施是 。
(1)图(Ⅰ)中瓶a内放入20 mL 6 mol·L-1盐酸,b是充气的气球,里边放有4 g碳酸钙粉末,将它紧紧套在瓶a口上,胶管c套在瓶的侧口,并用弹簧夹将d夹紧(瓶口和侧口都不漏气)。将图(Ⅰ)的装置放在托盘天平上称量,质量为W1。根据实验现象填写下列空白:
(1)把气球b中碳酸钙粉末小心地倒入瓶中,立即产生许多气泡,气球逐渐胀大(图Ⅱ)。反应结束后,再次称量,质量为W2。则W1和W2的关系是___________。
(2)取25 mL 6 mol·L-1NaOH溶液,先用滴管取少量NaOH溶液,滴管插入胶管c口(为方便操作,可以适当倾斜瓶a,注意防止漏气)。打开d,将溶液挤入瓶中,立即夹紧d,可以看到瓶内产生少量白色沉淀,轻轻摇动瓶a,沉淀随即消失。用同样方法再加入少量NaOH溶液,又产生白色沉淀,轻摇,沉淀又消失。使沉淀消失的反应的化学方程式是________________________________________________________________。
(3)将全部NaOH溶液很快加入瓶中,夹紧d,瓶内产生大量白色沉淀,不再溶解,此时瓶内温度___________(填“不变”“降低”或“升高”)。
(4)继续轻摇瓶a,气球逐渐缩小,直至恢复反应前的下垂状。写出这时发生的反应的化学方程式:____________________________;____________________________。
全世界每年因生锈损失的钢铁约占世界钢铁年产量的1/4。某学生想探究铁生锈的条件,他将干净的铁钉分别同时放入A、B、C三支试管中进行研究。
(1)请你帮助该学生完成下列实验设计的内容:
| 编号 |
操作方法 |
实验目的 |
| A |
探究铁在干燥空气中的生锈情况 |
|
| B |
放入铁钉,注入蒸馏水浸没铁钉,并用植物油液封 |
|
| C |
探究铁在有空气和水封时的生锈情况 |
(2)一周后,编号为___________的试管中的铁钉最易生锈。
(3)用相同材料制作,经过相同时间防锈处理的铁栏杆,安装在南方比安装在北方更易生锈,其原因是_____________________________________________。
(4)在焊接铁管时,为了使接口更加牢固,常用稀盐酸清洗接口处的铁锈,该反应的化学方程式为_______________________________________________。
电解原理在化学工业中有广泛应用。如下图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式为 。
在X极附近观察到的现象是 。
②Y电极上的电极反应式为 ,检验该电极反应产物的方法是 。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是 ,电极反应式为 。
②Y电极的材料是 ,电极反应式为 。
如下图在玻璃圆筒中盛有两种无色的互不相溶的中性液体。上层液体中插入两根石墨电极,圆筒内还放有一根下端弯成环状的玻璃搅棒,可以上下搅动液体。接通电源,阳极周围的液体呈现棕色,用搅棒上下剧烈搅动。静置后液体又分成两层,下层液体呈紫红色,上层液体几乎无色。根据上述实验回答: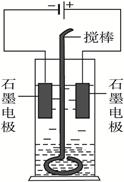
(1)阳极上的电极反应式为 。
(2)阴极上的电极反应式为 。
(3)原上层液体是 。
(4)原下层液体是 。
(5)搅拌后两层液体颜色发生变化的原因是 。
(6)要检验上层液体中含有的钾离子,其方法是 ,现象是 。
(10分)“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如右图所示的装置制取乙酸乙酯。完成下列问题: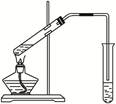
(1)写出制取乙酸乙酯的化学反应方程式__________________________________________。
(2)在大试管中配制一定比例的乙醇、乙酸和浓硫酸的混合液的方法是:________________。
(3)浓硫酸的作用是:①___________________________;②___________________________。
(4)饱和碳酸钠溶液的主要作用是
__________________________________________________。
(5)装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防止
___________________________________________。
(6)若要把制得的乙酸乙酯分离出来,应采用的实验操作是____________________________。
(7)做此实验时,有时还向盛乙酸和乙醇的试管里加入几块碎瓷片,其目的是
______________________________________________________________________________。
(8)生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,就达到了该反应的限度,即达到化学平衡状态。下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有(填序号) _________________。
①单位时间里,生成1 mol乙酸乙酯,同时生成1 mol水
②单位时间里,生成1 mol乙酸乙酯,同时生成1 mol乙酸
③单位时间里,消耗1 mol乙醇,同时消耗1 mol乙酸
④正反应的速率与逆反应的速率相等
⑤混合物中各物质的浓度不再变化