化学与社会、生产、生活紧切相关。下列说法正确的是( )
| A.石英只能用于生产光导纤维 |
| B.从海水中提取物质都必须通过化学反应才能实现 |
| C.为了增加食物的营养成分,可以大量使用食品添加剂 |
| D.“地沟油”禁止食用,但可以用来制肥皂 |
下列有关化学反应速率的说法中,正确的是()
| A.100 mL 2 mol/L的盐酸与锌反应时,加入适量的氯化钠溶液,生成氢气的速率不变 |
| B.用铁片和稀硫酸反应制取氢气时,改用铁片和浓硫酸可以加快产生氢气的速率 |
| C.二氧化硫的催化氧化是一个放热反应,所以升高温度,反应速率减慢 |
| D.汽车尾气中的CO和NO可以缓慢反应生成N2和CO2,减小压强,反应速率减慢 |
对可逆反应2SO2+O2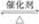 2SO3,下列叙述正确的是( )
2SO3,下列叙述正确的是( )
| A.反应达到平衡时,若两种反应物的转化率相等,则起始投入的n(SO2)∶n(O2)=2∶1 |
| B.反应达到平衡后,缩小容器体积,正反应速率加快,逆反应速率减慢,平衡正向移动 |
| C.反应达到平衡后,再加入催化剂,平衡不移动,反应速率不再加快 |
| D.当v正(SO2)∶v正(SO3)=1∶1时,说明该化学反应已经达到平衡 |
下列表格中的各种情况,可以用下图的曲线表示的是()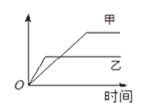
| 反应 |
纵坐标 |
甲 |
乙 |
|
| A |
相同质量的氨,在同一容器中 2NH3 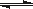 N2 + 3H2ΔH<0 N2 + 3H2ΔH<0 |
氨气的转化率 |
500℃ |
400℃ |
| B |
等质量钾、钠分别与足量水反应 |
H2质量 |
钠 |
钾 |
| C |
在体积可变的恒压容器中,体积比1︰3的N2、H2,N2 + 3H2 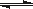 2NH3 2NH3 |
氨气的浓度 |
活性高的催化剂 |
活性一般的催化剂 |
| D |
2 molSO2和1 molO2,在相同温度下2SO2 + O2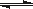 2SO3 2SO3 |
SO3物质的量 |
2个大气压 |
10个大气压 |
一定条件下,向某密闭容器中加入一定量的N2和H2发生可逆反应
N2(g)+3H2(g)  2NH3(g) ΔH = -92.2kJ•mol—1,测得0到10秒内,c(H2)减小了0.75mol•L—1,下列说法正确的是()
2NH3(g) ΔH = -92.2kJ•mol—1,测得0到10秒内,c(H2)减小了0.75mol•L—1,下列说法正确的是()
| A.10到15秒内c(NH3) 增加量等于0.25mol •L—1 |
| B.10秒内氨气的平均反应速率为0.025mol•L—1•s—1 |
| C.达平衡后,分离出少量NH3,v正增大 |
| D.该反应的逆反应的活化能不小于92.2kJ•mol—1 |
已知反应:①101 kPa时,2H2(g)+O2(g) ==2H2O(g) H=-483.6kJ/mol
H=-483.6kJ/mol
②稀溶液中,H+(aq)+OH-(aq)==H2O(l) H="-57.3" kJ/mol
H="-57.3" kJ/mol
又知由H2和O2两种气体反应生成1 mol液态水比生成1mol气态水多放出44kJ热量。下列结论中正确的是
| A.H2的燃烧热为285.8 kJ/mol |
| B.H2和O2反应生成液态水时的热化学方程式为H2(g) +1/2O2(g)=H2O(l)△H="-571.6" kJ/mol |
| C.稀硫酸与稀NaOH溶液反应的中和热为-57.3 kJ |
| D.稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量 |