我国是世界钢铁产量最大的国家,炼铁的主要原料是铁矿石。
(1)用赤铁矿石(主要成分为Fe2O3)炼铁的反应原理为:
(2)Fe2O3中铁元素的质量分数为:
(3)根据化学方程式计算:用含Fe2O360%的赤铁矿石800 t,理论上可炼出纯铁多少吨?
某市发现一大型铁矿,主体为磁铁矿。冶炼磁铁矿的反应为: 。用100t含Fe3O480%的磁铁矿石,理论上冶炼含杂质4%的生铁多少吨?(答案保留一位小数)
。用100t含Fe3O480%的磁铁矿石,理论上冶炼含杂质4%的生铁多少吨?(答案保留一位小数)
发射通讯卫星的火箭用联氨( )作燃料,用四氧化二氮(
)作燃料,用四氧化二氮(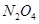 )助燃,生成物不会对大气造成污染。
)助燃,生成物不会对大气造成污染。
(1)反应的化学方程式为: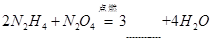 ,请在横线上填写化学式以完成该化学方程式。
,请在横线上填写化学式以完成该化学方程式。
(2)请计算9.6 kg  完全燃烧需要助燃物
完全燃烧需要助燃物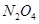 的质量。
的质量。
鸡蛋壳主要成分是碳酸钙。某兴趣小组为了测定鸡蛋壳中CaCO3的含量,现取15 g鸡蛋壳,捣碎,放在烧杯中,然后向其中加入80 g某浓度的稀盐酸,使之充分反应(鸡蛋壳中除CaCO3外的其他成分都不溶于水,且不与稀盐酸反应),测得烧杯中的反应剩余物的质量(m)与反应时间(t)的关系如图所示(忽略水蒸气的挥发),其中当反应进行到B点时,所用盐酸刚好消耗了加入量的一半。试计算(计算结果保留1位小数):(盐酸是HCl溶于水形成的溶液,反应中水不参加反应)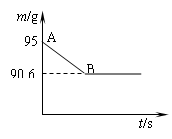
(1)产生CO2的质量为__________ g;
(2)该鸡蛋壳中CaCO3的质量分数;
为了测定某石灰石样品中碳酸钙的质量分数,某兴趣小组的同学进行了如下实验:取12.5g 石灰石样品,放入盛有100g稀盐酸的烧杯中,石灰石中的碳酸钙与盐酸恰好完全反应(假设石灰石中的杂质不与盐酸反应也不溶于水),烧杯内物质质量变为108.1g。
求:(1)根据质量守恒定律可知,反应中生成二氧化碳的质量为g.
(2)求该石灰石中碳酸钙的质量分数?
(3)将反应后的混合物过滤,求所得滤液的溶质质量分数?(计算结果保留一位小数)
石灰石样品的主要成分是CaCO3(已知其它杂质不与盐酸反应)。课外小组同学将50g盐酸分5次加入到20g该石灰石样品中,得到如下部分数据和图象:
请计算:
(1)石灰石样品中杂质的质量为g。
(2)所加盐酸的溶质质量分数。