元素的原子结构决定其性质和在周期表中的位置,下列说法中正确的是( )
A.元素周期表中位于金属和非金属分界线附近的元素属于过渡元素
B.某微粒的结构示意简图为 ,则该元素在周期表中位于第三周期、ⅥA族
,则该元素在周期表中位于第三周期、ⅥA族
C.过氧化氢电子式: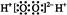
D Pd和
Pd和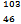 Pd互为同位素
Pd互为同位素
一定温度下,在固定容积、体积为2 L的密闭容器中充入1 mol N2和3 mol H2发生反应,当反应进行到10 s末时反应达到平衡,此时容器中c(NH3)=0.1mol·L-1。下列有关判断错误的是
| A.反应达平衡时N2的转化率为10% |
| B.反应进行到10 s末时,H2的平均反应速率是0.03 mol·(L·s)-1 |
| C.该反应达到平衡时,N2的平衡浓度为0.45 mol/L |
| D.该反应达到平衡时的压强是起始时压强的0.95倍 |
下列说法中正确的是
| A.将纯水加热至较高温度,Kw变大、pH变小、呈酸性 |
| B.保存FeSO4溶液时,应在其中加入稀HNO3以抑制Fe2+水解 |
| C.AlCl3溶液蒸干、灼烧至恒重,最终剩余固体是AlCl3 |
D.向0.1 mol·L-1氨水中加入少量水,pH减小,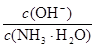 增大 增大 |
下列离子方程式书写正确的是
| A.鸡蛋壳和醋酸溶液的反应:CaCO3+2H+=Ca2++H2O+CO2↑ |
B.明矾水解的离子方程式:Al3++3H2O Al(OH)3↓+3H+ Al(OH)3↓+3H+ |
| C.向稀硫酸加入少量Ba(OH)2溶液:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O |
| D.向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
在下列溶液中,各组离子一定能够大量共存的是
| A.常温下,c(H+)/c(OH-)=1010的溶液:Na+、NH4+、SO42-、CH3COO- |
| B.滴入酚酞试液显红色的溶液:Na+、Ba2+、NO3-、Cl- |
| C.由水电离出的c(H+)=1×10-13mol/L的溶液:NH4+、K+、CO32-、Cl- |
| D.含有大量HCO3-的溶液:K+、Al3+、Cl-、Na+ |
设NA为阿伏加德罗常数的值,下列说法正确的是
| A.1L 1mol/L醋酸溶液中含有的离子总数为2NA |
| B.25℃时,pH=13的Ba(OH)2溶液中含有的OH-数目为0.1NA |
| C.100mL 1mol∙L-1的Na2CO3溶液中CO32-、HCO3-和H2CO3总数为0.1NA |
| D.0.1L 3mol·L-1的FeCl3溶液中含有的Fe3+数目为0.3 NA |