设NA为阿伏加德罗常数的值,下列叙述错误的是( )。
| A.标准状况下,22.4 L SO2和O2的混合气体中含有的氧原子数为2NA |
| B.标准状况下,22.4 L乙烯中含有共用电子对的数目为6NA |
| C.密闭容器中,3 mol H2和1 mol N2在高温、高压、催化剂的条件下充分反应后,容器内的气体分子总数为2NA |
| D.2.8 g的CO和2.8 g的N2所含质子数都为1.4NA |
已知:4NH3+5O2===4NO+6H2O,若反应速率分别用v(NH3) 、v(O2) 、v(NO) 、v(H2O)[来(mol·L-1· min-1)表示,则正确的关系是
min-1)表示,则正确的关系是
A.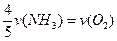 |
B.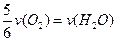 |
C.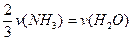 |
D.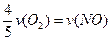 |
科学家近年来研制出一种新型细菌燃料电池,利用细菌将有机物转化为氢气,氢气进入 以磷酸为电解质溶液的燃料电池中发电,电池正极反应为
以磷酸为电解质溶液的燃料电池中发电,电池正极反应为
| A.H2+2OH--2c-===2H2O | B.O2+4H++4e-===2H2O |
C.H2-2e-====2H+ |
D.O2+2H2O+4e-===4OH- |
一定量的H2在一定条件下完全燃烧后,生成气态H2O,放出热量Q1,等质量的H2在相同条件下完全燃烧生成液态H2O,放出热量Q2,则Q1和Q2的关系是
| A.Q1> Q2 | B.Q1=Q2 | C.Q1<Q2 | D.无法确定 |
碱性电池具有容量大,放电电流大的特点,因而得到广泛应用,锌—锰碱性电池以氢氧化钾溶液为电解质溶液,电池总反应式为Zn(s)+2MnO2(s)+H2O(l)===Zn(OH)2(s)+Mn2O3(s)。下列说法中错误的是
| A.电池工作时,锌失去电子 |
| B.电池正极的电极反应式为2MnO2(s)+H2O(l)+2e-===Mn2O3(s)+2OH-(aq) |
| C.电池工作时,电子由正极通过外电路流向负极 |
| D.外电路中每通过0.2 mol电子,锌的质量理论上减少6.5 g |
A、B、C三种元素的原子序数依次a、b、c,它们的离子An+、Bn- 、Cm-具有相同的电子层结构,且n>m,则下列关系正确的是
、Cm-具有相同的电子层结构,且n>m,则下列关系正确的是
A.a>b>c B.a>c>b C.a="b+m+n" D.a=c-n-m