T ℃时在2 L的密闭容器中X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的浓度变化如图甲所示;若保持其他条件不变,反应温度分别为T1和T2时,Y的体积分数与时间的关系如图乙所示。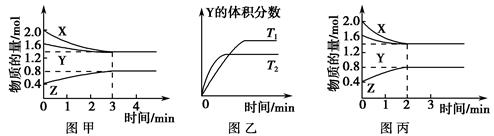
则下列结论正确的是(双选) ( )。
A.该反应可表示为3X(g)+Y(g) 2Z(g) 2Z(g) |
| B.若其他条件不变,升高温度,平衡将向逆反应方向移动 |
| C.若其他条件不变,开始时将该容器压缩为1 L,则反应将按图丙进行 |
| D.若其他条件不变,使用适当的催化剂,则反应可以按图丙进行 |
相同温度下,100mL 0.01 mol·L-1的醋酸溶液与10mL 0.1 mol·L-1的醋酸溶液相比较,下列数值前者大于后者的是
| A.中和时所需NaOH的量 | B.c(H+) |
| C.c(OH-) | D.c(CH3COOH) |
下列说法中正确的是
| A.凡是放热反应都是能自发进行的反应,而吸热反应都是非自发进行的反应 |
| B.自发反应一定是熵增大的反应,非自发反应一定是熵减小或不变的反应 |
| C.熵增加且放热的反应一定是自发反应 |
| D.非自发反应在任何条件下都不能发生 |
一个电池的总反应:Zn+Cu2+=Zn2++Cu,该反应的原电池的正确组成是
| A. | B. | C. | D. |
正极 Zn Cu Cu Ag
负极 Cu Zn Zn Cu
电解质溶液 CuCl2 H2SO4 CuSO4 AgNO3
反应PCl5(g) PCl 3(g)+Cl2(g)①
PCl 3(g)+Cl2(g)① 2HI(g)
2HI(g) H2(g)+I2(g)②
H2(g)+I2(g)② 2NO2(g)
2NO2(g) N2O4(g)③
N2O4(g)③ 在一定条件下,达到化学平衡时,反应物的转化率均是a%。若保持各自的温度不变、体积不变,分别再加入一定量的各自的反应物,则转化率
在一定条件下,达到化学平衡时,反应物的转化率均是a%。若保持各自的温度不变、体积不变,分别再加入一定量的各自的反应物,则转化率
| A.均不变 | B.①减少,②不变,③增大 |
| C.①增大,②不变,③减少 | D.均增大 |
下列操作会促进H2O的电离,且使溶液pH>7的是
| A.将纯水加热到90℃ | B.向水中加少量NaOH溶液 |
| C.向水中加少量Na2CO3溶液 | D.向水中加少量FeCl3溶液 |