短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法正确的是( )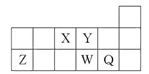
| A.元素X与元素Z的最高正化合价之和的数值等于8 |
| B.原子半径的大小顺序为:r(X)>r(Y)>r(Z)>r(W)>r(Q) |
| C.离子Y2-和Z3+的核外电子数和电子层数都不相同 |
| D.元素W的最高价氧化物对应的水化物的酸性比Q的强 |
准确称取6.0 g铝土矿样品(含Fe2O3),加入100 mL稀硫酸中,充分反应后向滤液中加入10 mol·L-1NaOH溶液,产生沉淀的质量和加入NaOH溶液体积之间的关系如图所示。则所用硫酸物质的量浓度为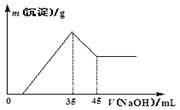
| A.1.75 mol·L-1 |
| B.3.50 mol·L-1 |
| C.0.85 mol·L-1 |
| D.无法确定 |
足量Zn粉与50ml、 0.1mol/L的稀硫酸充分反应。为了减慢此反应速率而不改变H2的产量,可以使用如下方法中的
①加Na2SO4溶液;②改用50ml、0.1mol/L的稀盐酸;③改用50ml、0.05mol/L的硝酸;
④加适量Na2CO3溶液;⑤减压;⑥冰水浴;
| A.①⑥ | B.①⑤⑥ | C.①②⑤⑥ | D.①②③⑤⑥ |
在一密闭容器中加入A、B、C三种气体,保持温度一定,在t1~t4时刻测得各物质的浓度如下表。据此判断下列结论正确的是
| 测定时刻/s |
t1 |
t2 |
t3 |
t4 |
| c(A)/(mol·L-1) |
6 |
3 |
2 |
2 |
| c(B)/(mol·L-1) |
5 |
3.5 |
3 |
3 |
| c(C)/(mol·L-1) |
1 |
2.5 |
3 |
3 |
A.在t3时刻反应已经停止
B.A的转化率比B的转化率低
C.t1至t2时刻该反应的速率为3mo1·L-1·s-1
D.该反应的化学方程式为2A(g)+B(g) C(g)
C(g)
下图是课外活动小组设计的用化学电源使LED灯发光的装置。下列说法错误的是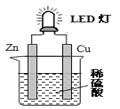
| A.铜片表面有气泡生成 |
| B.装置中存在“化学能→ 电能→ 光能”的转换 |
| C.如果将硫酸换成柠檬汁,导线中不会有电子流动 |
| D.如果将锌片换成铁片,电路中的电流方向不变 |
运用元素周期律分析下面的推断正确的是
| A.在氧气中,铷(Rb)的燃烧产物比钠的燃烧产物更复杂 |
| B.砹单质是一种有色固体,砹化氢很不稳定,砹化银是难溶于水的白色沉淀 |
| C.硫酸锶难溶于水,但易溶于盐酸 |
| D.硒化氢是无色、有毒、比硫化氢稳定的气体 |