已知离子方程式:As2S3+H2O+NO3—―→AsO43—+SO42—+NO↑+______K(未配平),下列说法错误的是( )。
| A.配平后水的化学计量数为4 |
| B.反应后溶液呈酸性 |
| C.配平后氧化剂与还原剂的物质的量之比为3∶28 |
| D.氧化产物为AsO43—和SO42— |
下列离子方程式正确的是
| A.Cl2通入水中:Cl2+H2O=2H+ +Cl-+ClO- |
| B.双氧水中加入稀硫酸和KI溶液:H2O2+2H++2I-=I2+2H2O |
C.用铜作电极电解CuSO4溶液:2Cu2++2H2O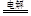 2Cu+O2↑+4H+ 2Cu+O2↑+4H+ |
| D.钢铁发生吸氧腐蚀时,铁作负极被氧化:Fe - 3e- = Fe3+ |
用NA表示阿伏加德罗常数的数值,下列说法正确的是
| A.46 g NO2和N2O4的混合物中含有的氮原子数为NA |
| B.常温常压下,22.4L乙烯中含极性共价键数目为5NA |
| C.1 L 0.1 mol/L的Fe2(SO4)3溶液中,Fe3+的数目为0.2 NA |
| D.1 mol羟基(—OH)中含电子数为10 NA |
下列有关物质的性质、应用等的说法正确的是()
| A.SiO2不能溶于任何酸 |
| B.在同浓度、同体积的碳酸钠和碳酸氢钠溶液中,各加入两滴酚酞,碳酸氢钠溶液中红色较深 |
| C.浓硫酸能干燥SO2等气体,说明浓硫酸具有吸水性 |
| D.自来水厂可用明矾对水进行消毒杀菌 |
在实验室,称取一定量的粗盐经溶解、过滤、结晶等操作,可得到较纯净的食盐。下列图示对应的操作不规范的是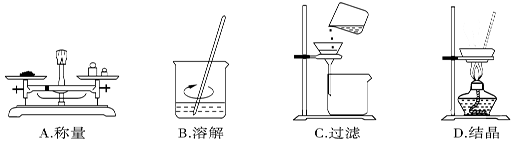
化学与生活密切相关,下列说法正确的是
| A.淀粉、油脂和蛋白质都是高分子化合物 |
| B.煤的气化和液化均属于化学变化 |
| C.雾霾的发生与汽车尾气的直接排放无关 |
| D.合成纤维和光导纤维都是新型无机非金属材料 |