下列各组变化中,ΔH或Q前者小于后者的一组是( )。
①CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH1
CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH2
②2H2(g)+O2(g)=2H2O(l) ΔH1
H2(g)+ O2(g)=H2O(l) ΔH2
O2(g)=H2O(l) ΔH2
③t ℃时,在一定条件下,将1 mol SO2和1 mol O2分别置于恒容和恒压的两个密闭容器中,达到平衡状态时放出的热量分别为Q1、Q2
④CaCO3(s)=CaO(s)+CO2(g) ΔH1
CaO(s)+H2O(l)=Ca(OH)2(s) ΔH2
| A.①②③ | B.②④ | C.②③④ | D.③④ |
据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电。其电池反应为:2CH3OH + 3O2 + 4 OH-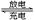 2CO32—+6H2O,则下列说法正确的是
2CO32—+6H2O,则下列说法正确的是
| A.构成该电池的正极和负极必须是两种活性不同的金属 |
| B.充电时有CH3OH生成的电极为阳极 |
| C.放电时负极的电极反应为:CH3OH-6e- +8OH- = CO32— + 6H2O |
| D.放电时,CO32—移向正极 |
下列有关以KOH溶液为电解液的氢氧燃料电池的叙述不正确的是
| A.正极反应式为:O2 + 2H2O +4e- =4OH- |
| B.工作一段时间后,电解液中KOH的物质的量浓度不变 |
| C.该燃料电池的总反应式为:2H2+O2=2H2O |
| D.用该电池电解CuCl2溶液,产生2.24LCl2(标准状况)时,有0.2mol电子转移 |
某原电池装置如图所示,电池总反应为:2Ag+Cl2=2AgCl,下列说法正确的是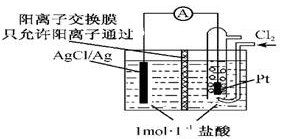
| A.正极反应为AgCl +e-=Ag +Cl- |
| B.放电时,交换膜右侧溶液中有大量白色沉淀生成 |
| C.若用NaCl溶液代替盐酸,则电池总反应随之改变 |
| D.当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.02 mol离子 |
通过NO传感器可监测NO的含量,其工作原理如图所示。下列说法错误的是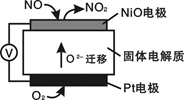
| A.该装置实现化学能向电能的转化 |
| B.该电池的总反应为2NO + O2 = 2NO2 |
| C.NiO电极的电极反应式: NO + O2- - 2e—= NO2 |
| D.当有2.24L的O2参与反应时,转移了0.4mole— |
液体燃料电池相比于气体燃料电池具有体积小等优点。一种以液态肼(N2H4)为燃料的电池装置如图所示,该电池用空气中的氧气作为氧化剂,KOH溶液作为电解质溶液。下列关于该电池的叙述正确的是: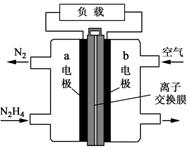
| A.b极发生氧化反应 |
| B.a极的反应式:N2H4+4OH--4e-=N2↑+4H2O |
| C.放电时,电流从a极经过负载流向b极 |
| D.其中的离子交换膜需选用阳离子交换膜 |