利用碳酸钠晶体(Na2CO3·10H2O)来配制0.5 mol/L的碳酸钠溶液1 000 mL,假如其他操作均是准确无误的,下列情况会引起配制溶液的浓度偏高的是( )
| A.称取碳酸钠晶体100 g |
| B.定容时俯视刻度线 |
| C.移液时,对用于溶解碳酸钠晶体的烧杯没有进行冲洗 |
| D.定容后,将容量瓶振荡均匀,静置发现液面低于刻度线,于是又加入少量水至刻度线 |
下列说法中,正确的是
| A.Na2O、Na2O2为相同元素组成的金属氧化物,都属于碱性氧化物 |
| B.SiO2、CO2均为酸性氧化物,均能与NaOH溶液反应生成盐和水 |
| C.FeO、Fe2O3均为碱性氧化物,与氢碘酸反应均只发生复分解反应 |
| D.将Fe(OH)3胶体和泥水分别进行过滤,分散质均不能通过滤纸孔隙 |
向一定量的Cu、Fe2O3的混合物中加入100 mL 2 mol·L-1的盐酸,恰好使混合物完全溶解,所得溶液中不含Fe3+,若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量为
| A.3.2 g | B.2.4 g | C.1.6 g | D.0.8 g |
下列物质的转化在给定条件下能实现的是
A. |
B. |
C.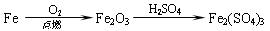 |
D.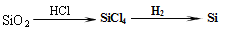 |
下列有关化学用语表示正确的是
| A.二氧化硅的分子式:SiO2 |
B.熔融状态下硫酸氢钾的电离方程式:KHSO4  K++HSO4- K++HSO4- |
C.甲基的电子式: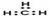 |
| D.HClO的结构式:H-Cl-O |
25℃时,用0.1mol·L-1的CH3COOH溶液滴定20mL0.1mol·L-1的NaOH溶液,当滴加VmLCH3COOH溶液时,混合溶液的pH=7。已知CH3COOH的电离平衡常数为Ka,忽略混合时溶液体积的变化,下列关系式正确的是
A.Ka= |
B.V= |
C.Ka=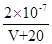 |
D.Ka= |