常见的五种盐A、B、C、D、E,它们的阳离子可能是Na+、 、Cu2+、Ba2+、Al3+、Ag+、Fe3+,阴离子可能是Cl-、
、Cu2+、Ba2+、Al3+、Ag+、Fe3+,阴离子可能是Cl-、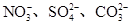 。已知:
。已知:
①五种盐均溶于水,水溶液均为无色。
②D的焰色反应呈黄色。
③A的溶液呈中性,B、C、E的溶液呈酸性,D的溶液呈碱性。
④若在这五种盐的溶液中分别加入Ba(NO3)2溶液,只有A、C的溶液不产生沉淀。
⑤若在这五种盐的溶液中,分别加入氨水,E和C的溶液中生成沉淀,继续加氨水,C中沉淀消失。
⑥把A的溶液分别加入到B、C、E的溶液中,均能生成不溶于稀硝酸的沉淀。
回答下列问题:
(1)五种盐中,一定没有的阳离子是_________________________________________________;
所含的阴离子相同的两种盐的化学式是_____________________________________________。
(2)D的化学式为_________,D溶液显碱性的原因是(用离子方程式表示)________________。
(3)A和C的溶液反应的离子方程式是______________________________________________。
E和氨水反应的离子方程式是______________________________________________________。
(4)若要检验B中所含的阳离子,正确的实验方法是__________________________________。
下图为相互串联的甲、乙两电解池试回答:
(1)若甲池利用电解原理在铁上镀银,则A是 (填电极材料),电极反应式是 ;B是 (填电极材料),电极反应式是 ,应选用的电解质溶液是 。
(2)乙池滴入少量酚酞试液,电解一段时间, (填“C”或“Fe”)极附近呈红色。
(3)若甲槽阴极增重43.2g,则乙槽中阳极上放出的气体在标况下的体积是 _________L。
某研究性学习小组拟取盐湖苦卤的浓缩液(富含K+、Mg2+、Br-、SO42-、Cl-等)来制取较纯净的氯化钾晶体及液溴,他们设计了如下流程。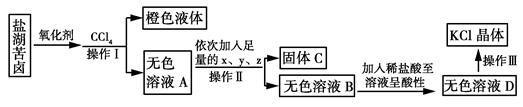
研究性学习小组查寻资料得知:Br-被氧化剂氧化成溴。溴不易溶于水而易溶于CCl4回答以下问题:
(1)操作Ⅰ的名称为______________;要从橙色液体中分离出溴,所采取的操作需要的主要玻璃仪器除酒精灯和温度计外,还有________ 。
(2)试剂x,y,z的化学式分别为x,_______ y z _;检验SO42-已除尽的方法是 。
(3)写出操作Ⅲ的具体操作步骤_________________________。
2 mol O3和3 mol O2的质量之比______________,分子数之比______________,同温同压的密度之比为______________,含氧原子数之比为______________,体积之比为______________。
有A、B、C三瓶失去标签的无色溶液:K2CO3、BaCl2、Na2SO4。首先不用其他试剂就可鉴别出的是 ,如要继续鉴别余下两种,还需要选用的试剂是 ,现象分别为 。
对于混合物的分离或提纯,常采用的方法有:①过滤、②蒸发、③蒸馏、④萃取、⑤加热分解等。下列各组混和物的分离或提纯应采用什么方法?(填序号)
(1)提取碘水中的碘 ____________________
(2)除去食盐溶液中的水 ______________________
(3)淡化海水 ______________________
(4)KCl中含有KClO3_____________________