氧化还原反应在生产、生活中具有广泛的用途,贯穿古今。
(1)水是人体的重要组成成分,是人体中含量最多的一种物质。而“四种基本反应类型与氧化还原反应的关系”也可用如图表达。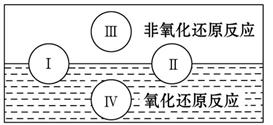
试写出有水参加的符合反应类型Ⅳ的一个化学方程式:________________________________,
其中水为_______剂。
(2)氯化铵常用作焊接。如:在焊接铜器时用氯化铵除去铜器表面的氧化铜以便焊接,其反应为:
_____CuO+_____NH4Cl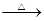 _____Cu+_____CuCl2+N2↑+_____H2O。
_____Cu+_____CuCl2+N2↑+_____H2O。
①配平此氧化还原反应方程式。
②该反应中,被氧化的元素是_______(填元素名称),氧化剂是_______(填化学式)。
(3)磷酸钙与焦炭、石英砂混合,在电炉中加热到1 500 ℃生成白磷,反应为:2Ca3(PO4)2+6SiO2=6CaSiO3+P4O10,10C+P4O10=P4+10CO。每生成1 mol P4时,就有_______mol电子发生转移。
某化学反应2A(g)  B(g)+D(g)在三种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
B(g)+D(g)在三种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
| 实验 |
  时间 时间浓度 温度 |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
| 1 |
800℃ |
1.0 |
0.80 |
0.67 |
0.57 |
0.50 |
0.50 |
0.50 |
| 2 |
800℃ |
c2 |
0.60 |
0.50 |
0.50 |
0.50 |
0.50 |
0.50 |
| 3 |
820℃ |
1.0 |
0.40 |
0.25 |
0.20 |
0.20 |
0.20 |
0.20 |
(1)在实验1,反应在10至20分钟时间内用A表示表示该反应的平均速率为_______
(2)在实验2,A的初始浓度c2=____mol/L,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是___________。
(3)比较实验3和1,则正反应是____反应(填吸热、放热),理由是___________________
对于可逆反应:2A(g)+3B(g)  xC(g)+D(g),已知A和B的起始浓度分别为5mol·L-1和3mol·L-1,反应开始到达平衡的时间是2 min,C的反应速率为0.5mol·L-1·min-1,平衡时D的浓度为0.5mol·L-1。求:
xC(g)+D(g),已知A和B的起始浓度分别为5mol·L-1和3mol·L-1,反应开始到达平衡的时间是2 min,C的反应速率为0.5mol·L-1·min-1,平衡时D的浓度为0.5mol·L-1。求:
(1)x=
(2)B的平衡浓度为
(3)该反应平衡常数为 。(只要求写数值且保留一位有效数字)
已知下列热化学方程式:①H2(g) + O2(g) =H2O(l);ΔH="-285" kJ·mol-1
O2(g) =H2O(l);ΔH="-285" kJ·mol-1
②H2(g) + O2(g) =H2O(g);ΔH="-241.8" kJ·mol-1
O2(g) =H2O(g);ΔH="-241.8" kJ·mol-1
③C(s) + O2(g) =CO(g);ΔH="-110.5" kJ·mol-1
O2(g) =CO(g);ΔH="-110.5" kJ·mol-1
④ C(s) +O2(g) =CO2(g);ΔH="-393.5" kJ·mol-1
回答下列问题:
(1)H2的燃烧热为C的燃烧热为。
(2)燃烧10gH2生成液态水,放出的热量为。
(3)写出CO燃烧的热化学方程式。
实验室欲用NaOH固体配制1.0mol/L的NaOH溶液480mL:
(1)配制时,必须使用的玻璃仪器有________、________、________、________。
(2)要完成本实验该同学应称出NaOH________g。
(3)某同学欲称量NaOH的质量,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图,烧杯的实际质量为________g。
(4)使用容量瓶前必须进行的一步操作是________。
(5)在配制过程中,其他操作都是正确的,下列操作会引起误差偏高的是________。
①没有洗涤烧杯和玻璃棒 ②转移溶液时不慎有少量洒到容量瓶外面
③容量瓶不干燥,含有少量蒸馏水 ④定容时俯视刻度线
⑤未冷却到室温就将溶液转移到容量瓶并定容
⑥定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线。
标准状况下,① 4g氢气 ② 33.6L甲烷(CH4) ③ 6.02×1023个水分子中,含分子数最多的是(填写序号,下同)_____,含原子数最多的是_____,质量最大的是______,体积最小的是______。